Коррозия металлов и способы защиты от нее
| Коррозия – это процесс разрушения металлов и металлических конструкций под воздействием различных факторов окружающей среды – кислорода, влаги, вредных примесей в воздухе. |
Коррозионная стойкость металла зависит от его природы, характера среды и температуры.
- Благородные металлы не подвергаются коррозии из-за химической инертности.
- Металлы Al, Ti, Zn, Cr, Ni имеют плотные газонепроницаемые оксидные плёнки, которые препятствуют коррозии.
- Металлы с рыхлой оксидной плёнкой – Fe, Cu и другие – коррозионно неустойчивы. Особенно сильно ржавеет железо.
Различают химическую и электрохимическую коррозию.
Химическая коррозия сопровождается химическими реакциями. Как правило, химическая коррозия металлов происходит при действии на металл сухих газов, её также называют газовой. |
3Fe + 2O2 = Fe3O4
При химической коррозии также возможны процессы:
Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3
Как правило, такие процессы протекают в аппаратах химических производств.
| Электрохимическая коррозия – это процесс разрушения металла, который сопровождается электрохимическими процессами. Как правило, электрохимическая коррозия протекает в присутствии воды и кислорода, либо в растворах электролитов. |
В таких растворах на поверхности металла возникают процессы переноса электронов от металла к окислителю, которым является либо кислород, либо кислота, содержащаяся в растворе.
При этом электродами являются сам металл (например, железо) и содержащиеся в нем примеси (обычно менее активные металлы, например, олово).
В таком загрязнённом металле идёт перенос электронов от железа к олову, при этом железо (анод) растворяется, т.е. подвергается коррозии:
Fe –2e = Fe 2+
На поверхности олова (катод) идёт процесс восстановления водорода из воды или растворённого кислорода:
2H+ + 2e → H2
O2 + 2H2O + 4e → 4OH–
| Например, при контакте железа с оловом в растворе соляной кислоты происходят процессы: |
Анод: Fe –2e → Fe 2+
Катод: 2H+ + 2e → H2
Суммарная реакция: Fe + 2H+ → H2 + Fe2+
Если реакция проходит в атмосферных условиях в воде, в ней участвует кислород и происходят процессы:
Анод: Fe –2e → Fe 2+
Катод: O2 + 2H2O + 4e → 4OH–
Суммарная реакция:
Fe 2+ + 2OH – → Fe(OH)2
4Fe(OH)2 + O2+ 2H2O → 4Fe(OH)3
При этом образуется ржавчина.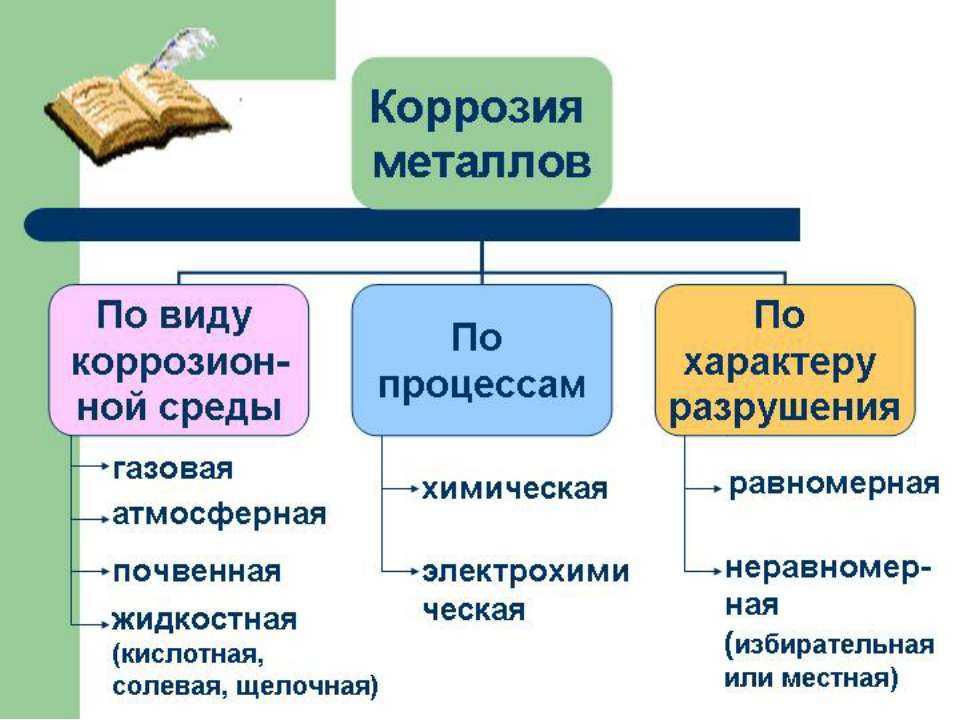
Защитные покрытия
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
- Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
- Покрытие краской, лаками, смазками.
- Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Создание сплавов, стойких к коррозии
Физические свойства сплавов могут существенно отличаться от свойств чистых металлов. Добавление некоторых металлов может приводить к повышению коррозионной стойкости сплава. Например, нержавеющая сталь, новые сплавы с большой коррозионной устойчивостью.
Изменение состава среды
Коррозия замедляется при добавлении в среду, окружающую металлическую конструкцию, ингибиторов коррозии. Ингибиторы коррозии — это вещества, подавляющие процессы коррозии.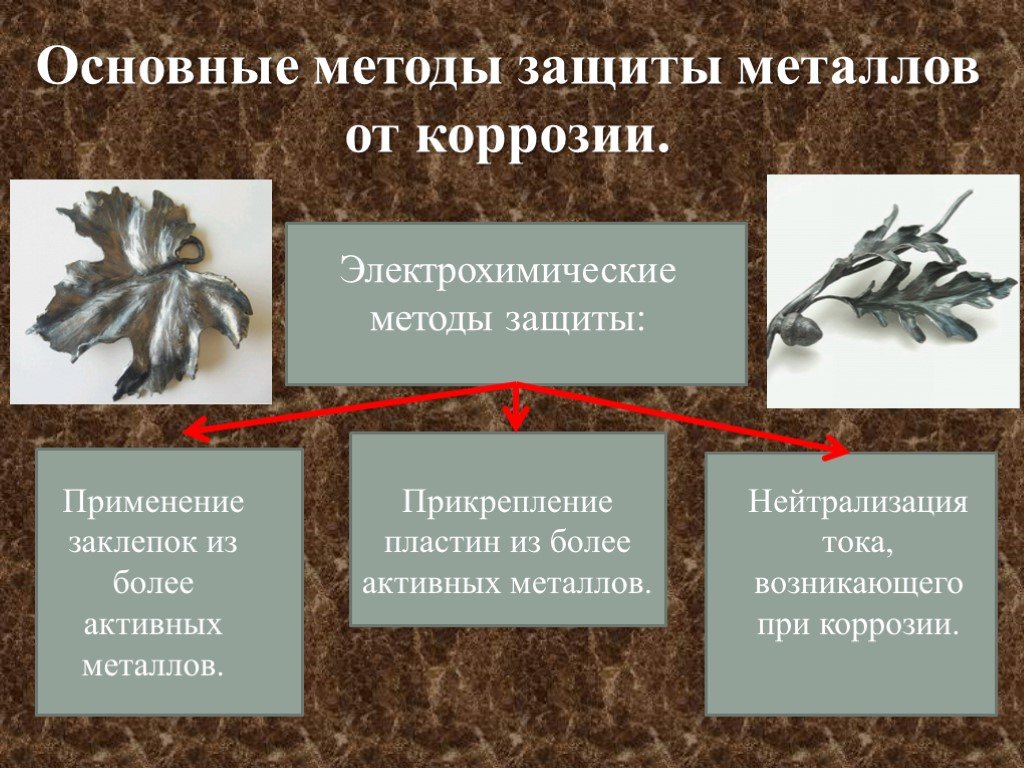
Электрохимические методы защиты
Протекторная защита: при присоединении к металлической конструкции пластинок из более активного металла – протектора. В результате идёт разрушение протектора, а металлическая конструкция при этом не разрушается.
Понравилось это:
Нравится Загрузка…
Коррозия металлов — что это такое? Виды и примеры
Поможем понять и полюбить химию
Начать учиться
Всякое явление или процесс вокруг нас связан с химией. Скажем, ржавление железа. Хоть раз в жизни вы наверняка задумывались, почему одни металлы ржавеют и разрушаются, а другие — нет. И что такого особенного в нержавеющей стали, что этот процесс ей нипочем? Обо всем это мы и поговорим в сегодняшней статье.
Коротко о главном
Коррозия металлов или ржавление в химии — это явление, которое возникает из-за взаимодействия металлической пластинки с веществами окружающей среды (кислородом воздуха или кислотами, с которыми может реагировать металлическое изделие).
Обычно окисляются металлы, включая железо, которые находятся левее водорода в ряду напряжений.
Чаще всего встречаются химическая и электрохимическая коррозии. Чтобы понять, чем они отличаются друг от друга, давайте сравним их по нескольким критериям в таблице ниже.
Таблица 1. Сравнение химической и электрохимической коррозии металлов |
||
|---|---|---|
Признаки сравнения |
Химическая коррозия |
Электрохимическая коррозия |
Определение |
Разрушение металлов в из-за взаимодействия с газами или растворами, которые не проводят электрический ток |
Разрушение металла, при котором возникает электрический ток в воде или среде другого электролита |
Агрессивные реагенты |
O2, пары H2O, CO2, SO2, Cl2 |
Растворы электролитов |
Примеры |
3Fe + 2O2 → Fe3O4 |
4Fe + 3O2 + 6H2O = 4 Fe(OH)3 При контакте железа с цинком коррозии подвергается цинк: А (+) на цинке: Zn0 — 2e— = Zn2+. К (–) на железе: 2H+ + 2e— = H2. |
Защитить металл от коррозии можно по-разному: покрытием защитными материалами, электрохимическими методами, шлифованием и т. д. Далее — подробно обо всем этом.
Узнай, какие профессии будущего тебе подойдут
Пройди тест — и мы покажем, кем ты можешь стать, а ещё пришлём подробный гайд, как реализовать себя уже сейчас
Что такое коррозия
Коррозия — это самопроизвольное разрушение элементов, чаще всего металлов, под действием химического или физико-химического влияния окружающей среды.
Иными словами, из-за химического воздействия железо начинает ржаветь. Это весьма сложный процесс, который состоит из несколько этапов. Но суммарное уравнение коррозии выглядит так:
4Fe + 6H2O (влага) + 3O2 (воздух) = 4Fe(OH)3.
Часто под коррозией понимают химическую реакцию между материалом и средой либо между их компонентами, которая протекает на границе раздела фаз. Обычно это окисление металла. Например:
3Fe + 2О2 = Fe3O4;
Fe + H2SO4 = FeSО4 + Н2.
Некоторые металлы, даже активные, покрываются плотной оксидной пленкой при коррозии. Это одна из их характерных черт. Оксидная пленка не дает окислителям проникнуть в более глубокий слой и поэтому защищает металл от коррозии. Алюминий обычно устойчив при контакте с воздухом и водой, даже горячей. Тем не менее, если поверхность алюминия покрыть ртутью, то образуется амальгама. Она разрушает оксидную пленку, и алюминий начинает быстро превращаться в белые хлопья метагидроксида алюминия:
Коррозии подвергаются и многие малоактивные металлы. Например, поверхность медного изделия покрывается патиной — зеленоватым налетом. Это происходит потому, что на ней образуются смеси основных солей.
Например, поверхность медного изделия покрывается патиной — зеленоватым налетом. Это происходит потому, что на ней образуются смеси основных солей.
Виды коррозии металлов
Химическая коррозия
Химическая коррозия — это процесс разрушения металла, который связан с реакцией между металлом и коррозионной средой.
Химическая коррозия протекает без воздействия электрического тока, и в результате этой реакции металлы окисляются. Этот вид коррозии можно разделить на два подвида:
газовая коррозия — металл корродирует под воздействием различных газов при высоких температурах;
коррозия в жидкостях — неэлектролитах.
Их них более распространенной считают газовую коррозию. Она протекает во время прямого контакта твердого тела с активным газом воздуха. Чаще всего это кислород. В результате на поверхности тела образуется пленка продуктов химической реакции между веществом и газом. Дальше эта пленка мешает контакту корродирующего материала с газом. При высоких температурах газовая коррозия развивается интенсивно. Возникшая при этом пленка называется окалиной, которая со временем становится толще.
В результате на поверхности тела образуется пленка продуктов химической реакции между веществом и газом. Дальше эта пленка мешает контакту корродирующего материала с газом. При высоких температурах газовая коррозия развивается интенсивно. Возникшая при этом пленка называется окалиной, которая со временем становится толще.
Важную роль в процессе коррозии играет состав газовой среды. Но для каждого металла он индивидуален и изменяется с переменой температур.
Электрохимическая коррозия
Электрохимическая коррозия — это разрушение металла, которое протекает при его взаимодействии с окружающей средой электролита.
Этот вид коррозии считают наиболее распространенным. Самым важным происхождением электрохимической коррозии является то, что металл неустойчив в окружающей среде с точки зрения термодинамики. Вот несколько ярких примеров этой реакции: ржавчина в трубопроводе, на обшивке днища морского судна и на различных металлоконструкциях в атмосфере.
В механизме электрохимической коррозии обычно выделяют два направления: гомогенное и гетерогенное. Разберем их подробнее в таблице ниже.
Гомогенный механизм электрохимической коррозии |
Гетерогенный механизм электрохимической коррозии |
|---|---|
Поверхность металла рассматривается как однородный слой. |
У твердых металлов поверхность неоднородна из-за структуры сплава, в котором атомы по-разному расположены в кристаллической решетке. |
Растворение металла происходит из-за термодинамической возможности для катодного или анодного процессов. |
Неоднородность можно наблюдать при наличии в сплаве каких-либо включений. |
Скорость, с которой протекает электрохимическая коррозия, зависит от времени протекания процесса. |
В электрохимической коррозии протекает одновременно два процесса на аноде и на катоде, которые зависят друг от друга. Растворение основного металла происходит только на анодах. Анодный процесс заключается в том, что ионы металла отрываются и переходят в раствор:
Fe → Fe2+ + 2e.
В результате происходит реакция окисления металла. В данном случае анод заряжается отрицательно.
При катодном процессе избыточные электроны переходят в молекулы или атомы электролита, которые, в свою очередь, восстанавливаются. На катоде идет реакция восстановления. Он носит заряд положительного электрода.
O2 + 2H2O + 4e → 4OH—
2H+ + 2e → H2
Торможение одного процесса приводит к торможению и другого процесса. Окисление металла может происходить только в анодном процессе.
Окисление металла может происходить только в анодном процессе.
Как защитить металлы от коррозии
От коррозии можно и нужно защищаться. Чтобы уберечь металлы от этой реакции, их покрывают защитными материалами, обрабатывают электрохимическими методами, шлифованием и т. д. Рассмотрим все эти способы подробнее.
Способ № 1. Защитные покрытия.
Для защиты от коррозии металлические изделия покрывают другим металлом, т. е. производят никелирование, хромирование, цинкование, лужение и т. д. Еще один вариант защиты — покрыть поверхность металла специальными лаками, красками, эмалями.
Способ № 2. Легирование.
Легирование — это введение добавок, которые образуют защитный слой на поверхности металла. Например, при легировании железа хромом и никелем получают нержавеющую сталь.
Способ № 3. Протекторная защита.
Протекторная защита.
Протекторная защита — это способ уберечь металл от коррозии, при котором металлическое изделие соединяют с более активным металлом. Этот второй металл в итоге и разрушается в первую очередь.
Способ № 4. Электрохимическая защита.
Чтобы защитить металлы от электрохимической коррозии, нейтрализуют ток, который возникает при ней. Это делают с помощью постоянного тока, который пропускают в обратном направлении.
Способ № 5. Изменение состава среды путем добавления ингибиторов.
Для защиты от коррозии используют специальные средства, которые ее замедляют — ингибиторы. Они изменяют состояние поверхности металла — образуют труднорастворимые соединения с катионами металла. Защитные слои, образованные ингибиторами, всегда тоньше наносимых покрытий.
Способ № 6. Замена корродирующего металла на другие материалы: керамику и пластмассу.
Способ № 7. Шлифование поверхностей изделия.
Проверьте себя
Что такое коррозия?
Где в повседневной жизни можно встретить ржавление железа и других металлов? Приведите примеры.
Гидроксид железа Fe(OH)3 называют:
а ржавчина;
б) окалина;
в) патина.
Что является причиной возникновения коррозии?
Чем отличаются химический и электрохимический типы коррозии?
Что такое коррозионная среда?
Узнайте все о коррозии металлов и разберитесь в других темах за 9 класс на онлайн-курсах по химии в Skysmart! Наши преподаватели помогут выяснить, где скрываются пробелы в знаниях, и восполнить их. Никаких скучных задач и сухих лекций — только интерактивные упражнения, опыты и теория простым языком. Все это поможет разобраться даже в тех темах, которые не давались в школе. Ждем на бесплатном вводном уроке!
Никаких скучных задач и сухих лекций — только интерактивные упражнения, опыты и теория простым языком. Все это поможет разобраться даже в тех темах, которые не давались в школе. Ждем на бесплатном вводном уроке!
Татьяна Сосновцева
К предыдущей статье
Водородный показатель pH
К следующей статье
Химическое равновесие
Получите план обучения, который поможет понять и полюбить химию
На вводном уроке с методистом
Выявим пробелы в знаниях и дадим советы по обучению
Расскажем, как проходят занятия
Подберём курс
Коррозия и как защитить от нее металл — Блог
Коррозия — это процесс расхода строительных материалов при химическом воздействии жидкостей, разрушительно воздействующий на металлы и неорганические металлы, а также участвующий в разложении органических материалов.
Коррозия и защита металлов от коррозии
Коррозия — это нежелательный процесс, с которым мы сталкиваемся ежедневно и который связан с реакцией металла и окружающей средой, в которой он находится.
Это опасно по нескольким причинам, и одна из основных — это; повреждая металл до такой степени, что изменяются некоторые его механические свойства.
Один из курьезов, связанных с коррозией и важностью антикоррозионной защиты; заключается в том, что коррозия ежегодно приводит к потере 3,5% мирового ВВП.
Однако не все металлы подвержены коррозии. Такие металлы, как цинк, никель, олово, алюминий, золото, платина и легированная сталь; где процентное содержание хрома превышает 13%, являются коррозионностойкими.
Кроме того, некоторые драгоценные металлы, такие как золото и платина, также устойчивы к коррозии.
Виды коррозии
Если разделить коррозию на виды, то получится:
- Общая коррозия которая поражает всю поверхность металла.
 Такая коррозия одинаково повреждает всю поверхность материала. Общая коррозия также известна как «ржавчина».
Такая коррозия одинаково повреждает всю поверхность материала. Общая коррозия также известна как «ржавчина».
- Точечная коррозия – это такая коррозия, которая возникает в небольших углублениях на поверхности материала, которые со временем превращаются в более крупные отверстия.
- Межкристаллитная коррозия проникает в материал и поэтому практически незаметна на поверхности.
- Избирательная коррозия , которая поражает только отдельные компоненты сложного материала. Этот тип коррозии начинается на поверхности материала, а затем проникает внутрь и атакует с разной скоростью.
- Коррозионное растрескивание под напряжением – такая коррозия, которая возникает, когда материал подвергается пределу прочности при растяжении; а также действие агрессивного агента
Защита от коррозии
Для защиты от коррозии были разработаны многочисленные методы, которые можно разделить на:
- Защита от коррозии с помощью покрытия все примеси, такие как жир и коррозия.
 Подготовка поверхности обычно осуществляется шлифованием, крацеванием, полированием, пескоструйной обработкой или промоканием. Что касается покрытий, наносимых на материал, то они могут быть металлическими, эмалированными, т.е. наиболее известными и наиболее распространенными, лакокрасочными
Подготовка поверхности обычно осуществляется шлифованием, крацеванием, полированием, пескоструйной обработкой или промоканием. Что касается покрытий, наносимых на материал, то они могут быть металлическими, эмалированными, т.е. наиболее известными и наиболее распространенными, лакокрасочными
- Электрохимическая защита от коррозии – Электрохимическая защита от коррозии проводится для труднодоступных и непростых в обслуживании металлов. Электрохимическая защита от коррозии применяется для защиты нефтепроводов, судов, резервуаров и других устройств, используемых в промышленности
- Конструктивные меры – защита от коррозии, связанная с выбором тех материалов, которые обладают определенными свойствами, снижающими вероятность коррозии
- Защита от изменения обстоятельств – Этот вид защиты от коррозии осуществляется путем изменения окружающих факторов, участвующих в процессе повреждения.
 В этом виде защиты следует упомянуть ингибиторы коррозии, которые в малых дозах предотвращают процесс коррозии .
В этом виде защиты следует упомянуть ингибиторы коррозии, которые в малых дозах предотвращают процесс коррозии .
Гальванизация как форма защиты от коррозии
Одним из наиболее известных методов защиты металла от коррозии является гальванизация. Цинкование – это не что иное, как нанесение тонкого слоя цинка на материал, который нужно защитить от коррозионного воздействия.
Гальванизация — наиболее распространенный метод защиты металла. Процесс цинкования осуществляется погружением металлов в расплавленный цинк, электрохимическим процессом, напылением цинка и диффузией цинка.
Однако наиболее часто используемым методом цинкования является процесс горячего цинкования, при котором металл погружается в цинк с температурой 450°C. Это также один из старейших методов защиты металла, очень экономичный и простой.
После оцинковки металл защищен почти на весь срок службы.
Введение в коррозию и защиту металлов
Авторы:
- Госта Вранглен
-
Госта Вранглен
Посмотреть публикации автора
Вы также можете искать этого автора в пабмед Google Scholar
‘)
var head = document.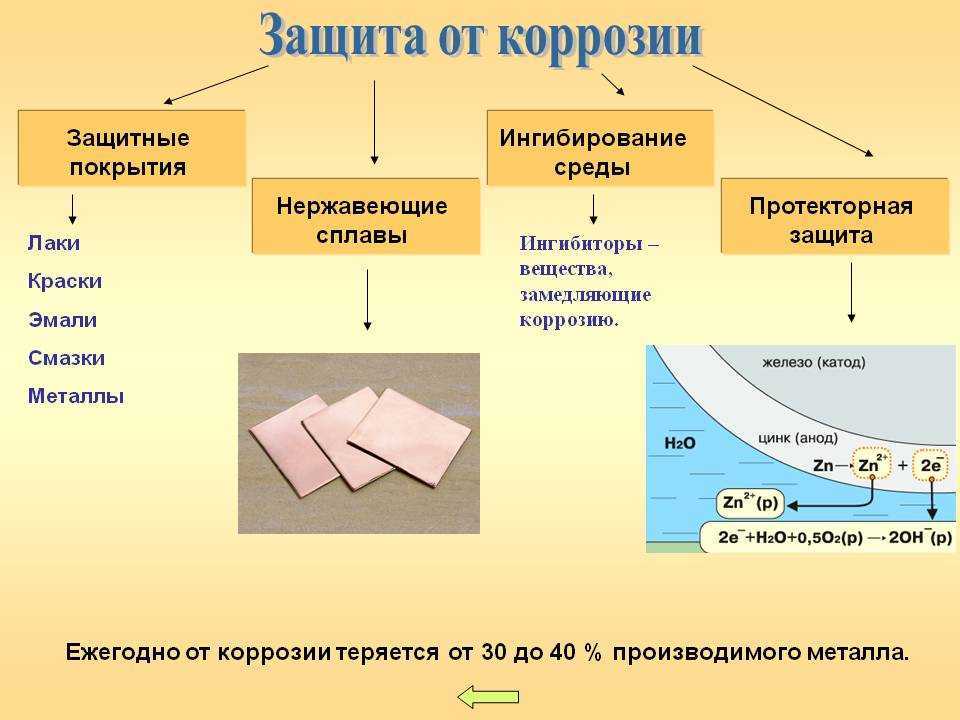 getElementsByTagName(«head»)[0]
var script = document.createElement(«сценарий»)
script.type = «текст/javascript»
script.src = «https://buy.springer.com/assets/js/buybox-bundle-abe5f44a67.js»
script.id = «ecommerce-scripts-» + метка времени
head.appendChild (скрипт)
var buybox = document.querySelector(«[data-id=id_»+ метка времени +»]»).parentNode
var сейчас = новая дата().getTime()
вар начало = 1650956400000
вар конец = 1652338800000
var isMeasuringTime = сейчас > начать && сейчас -1
;[].slice.call(buybox.querySelectorAll(«.опция покупки»)).forEach(функция (опция, индекс) {
var toggle = option.querySelector(priceNS + «.buying-option-price»)
var form = option.querySelector(«.форма-варианта-покупки»)
var priceInfo = option.
getElementsByTagName(«head»)[0]
var script = document.createElement(«сценарий»)
script.type = «текст/javascript»
script.src = «https://buy.springer.com/assets/js/buybox-bundle-abe5f44a67.js»
script.id = «ecommerce-scripts-» + метка времени
head.appendChild (скрипт)
var buybox = document.querySelector(«[data-id=id_»+ метка времени +»]»).parentNode
var сейчас = новая дата().getTime()
вар начало = 1650956400000
вар конец = 1652338800000
var isMeasuringTime = сейчас > начать && сейчас -1
;[].slice.call(buybox.querySelectorAll(«.опция покупки»)).forEach(функция (опция, индекс) {
var toggle = option.querySelector(priceNS + «.buying-option-price»)
var form = option.querySelector(«.форма-варианта-покупки»)
var priceInfo = option. querySelector(priceNS + «.price-info»)
если (allOptionsInitiallyCollapsed || узкаяBuyboxArea && индекс > 0) {
toggle.setAttribute («ария-расширенная», «ложь»)
form.hidden = «скрытый»
priceInfo.hidden = «скрытый»
} еще {
переключить.щелчок()
}
})
}
начальное состояниеОткрыть()
если (window.buyboxInitialized) вернуть
window.buyboxInitialized = истина
initKeyControls()
если (window.fetch && isMeasuringTime) {
var свернутый = buybox.querySelector(«.buying-option.expanded») === ноль
var metricsAppendix = «»
metricsAppendix += «&discount=» + (buybox.querySelector(«.
querySelector(priceNS + «.price-info»)
если (allOptionsInitiallyCollapsed || узкаяBuyboxArea && индекс > 0) {
toggle.setAttribute («ария-расширенная», «ложь»)
form.hidden = «скрытый»
priceInfo.hidden = «скрытый»
} еще {
переключить.щелчок()
}
})
}
начальное состояниеОткрыть()
если (window.buyboxInitialized) вернуть
window.buyboxInitialized = истина
initKeyControls()
если (window.fetch && isMeasuringTime) {
var свернутый = buybox.querySelector(«.buying-option.expanded») === ноль
var metricsAppendix = «»
metricsAppendix += «&discount=» + (buybox.querySelector(«. Цена-кампания-покупки-варианта»).className.indexOf(«со скидкой») !== -1).toString()
metricsAppendix += «&metricsGroup=» + кампанияPricesMetricsGroup
metricsAppendix += «&collapsed=» +collapsed.toString()
window.fetch(«https://test-buckets.springer.com/log?v3&time=» + сейчас + приложение metrics)
.затем (функция (разрешение) {
вернуть рез.текст()
})
.поймать (функция () {
})
}
})()
Цена-кампания-покупки-варианта»).className.indexOf(«со скидкой») !== -1).toString()
metricsAppendix += «&metricsGroup=» + кампанияPricesMetricsGroup
metricsAppendix += «&collapsed=» +collapsed.toString()
window.fetch(«https://test-buckets.springer.com/log?v3&time=» + сейчас + приложение metrics)
.затем (функция (разрешение) {
вернуть рез.текст()
})
.поймать (функция () {
})
}
})()
Об этой книге
Коррозию можно определить как непреднамеренное воздействие на материал в результате реакции с окружающей средой. Этот термин может относиться к процессу или к ущербу, причиняемому таким процессом. Согласно этому общему определению материалы, отличные от металлов, такие как керамика, пластмассы или бетон, также могут подвергаться коррозии (или коррозии). Однако, когда материал не упоминается конкретно, обычно подразумевается, что металл подвергается воздействию. Именно в этом ограниченном смысле этот термин используется в этой книге. Есть веские причины рассматривать коррозию металлов отдельно от износа или распада других материалов. Поскольку металлы обладают высокой электропроводностью, их коррозия обычно носит электрохимический характер. Химический износ непроводящих электричество материалов, таких как пластмассы и керамика, определяется другими физико-химическими принципами. Коррозии металлов в настоящее время необходимо уделять больше внимания, чем раньше, в связи с 1. Увеличением использования металлов во всех областях техники. 2. Использование для специальных приложений, например. в области атомной энергетики, редких и дорогих металлов, сохранение которых требует особых мер предосторожности. 3. Более агрессивная среда из-за возрастающего загрязнения воздуха и воды. 4. Использование металлических конструкций более тонких размеров, которые не выдерживают коррозионного воздействия в той же степени, что и тяжелые конструкции, использовавшиеся в старину.
Однако, когда материал не упоминается конкретно, обычно подразумевается, что металл подвергается воздействию. Именно в этом ограниченном смысле этот термин используется в этой книге. Есть веские причины рассматривать коррозию металлов отдельно от износа или распада других материалов. Поскольку металлы обладают высокой электропроводностью, их коррозия обычно носит электрохимический характер. Химический износ непроводящих электричество материалов, таких как пластмассы и керамика, определяется другими физико-химическими принципами. Коррозии металлов в настоящее время необходимо уделять больше внимания, чем раньше, в связи с 1. Увеличением использования металлов во всех областях техники. 2. Использование для специальных приложений, например. в области атомной энергетики, редких и дорогих металлов, сохранение которых требует особых мер предосторожности. 3. Более агрессивная среда из-за возрастающего загрязнения воздуха и воды. 4. Использование металлических конструкций более тонких размеров, которые не выдерживают коррозионного воздействия в той же степени, что и тяжелые конструкции, использовавшиеся в старину.


