Таблица совместимости металлов и сплавов
Опубликовано 2023-01-13
- Таблица электрохимической совместимости металлов
- Способы защиты от контактной коррозии
Гальваническая пара, которую погружают в кислотный или щелочной раствор, будет разрушаться под воздействием кислорода (корродировать). Такой процесс называется гальванической коррозией.
Соединения разных металлов под действием атмосферы подвержены коррозии, однако некоторые пары металлов окисляются намного сильнее и быстрее.
Несовместимые гальванические пары следующие:
- Алюминии и его сплавы.
- Медь, все сплавы на ее основе, золото, платина, олово, никель, хром, нелегированная сталь.
- Магниево-алюминиевые сплавы.
- Цинк и сплавы.
- Никель, хром, серебро, золото, родий, палладий.
- Титан и его сплавы.
- Алюминий и его сплавы.

Нельзя механически соединять детали, у которых разный электрохимический потенциал. Например, латунные детали алюминиевыми заклепками соединять недопустимо. Чтобы выбрать подходящий материал, используйте таблицу совместимости металлов и сплавов.
Таблица электрохимической совместимости металлов
| Материал | Алюминий | Бронза | Дюраль | Латунь | Медь | Никель | Олово | Оловянно-свинцовый сплав (припой ПОС) | Сталь нелегированная (углеродистая) / чугун | Хром | Цинк |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Алюминий | Совм | Не совм | Совм | Не совм | Не совм | Не совм | Не совм | Не совм | Совм | Не совм | Совм |
| Бронза | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Дюралюминий | Совм | Не совм | Совм | Не совм | Не совм | Не совм | Не совм | Не совм | Совм | Не совм | Совм |
| Латунь | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Медь | Не совм | Совм | Не совм | Совм | Совм | Совм | Пайка | Пайка | Не совм | Совм | Не совм |
| Никель | Не совм | Совм | Не совм | Совм | Совм | Пайка | Пайка | Совм | нет данных | Совм | |
| Олово | Не совм | Пайка | Не совм | Пайка | Пайка | Пайка | Совм | Совм | Совм | нет данных | Совм |
|
Оловянно-свинцовый сплав (припой ПОС) |
Не совм | Пайка | Не совм | Пайка | Пайка | Пайка | Совм | Совм | Совм | нет данных | Совм |
| Сталь нелегированная (углеродистая)/ чугун | Совм | Не совм | Совм | Не совм | Не совм | Совм | Совм | Совм | Совм | Совм | Совм |
| Хром | Не совм | Совм | Не совм | Совм | Совм | нет данных | нет данных | нет данных | Совм | Совм | Совм |
| Цинк | Совм | Не совм | Совм | Не совм | Не совм | Совм | Совм | Совм | Совм | Совм | Совм |
- Совм – совместимые
- Не совм – несовместимые
- П – совместимые при пайке, но несовместимые при непосредственном соприкосновении, так как образуют гальваническую пару
Способы защиты от контактной коррозии
Электрическая совместимость металлов – это возможность создать соединение без гальванической пары (анода и катода).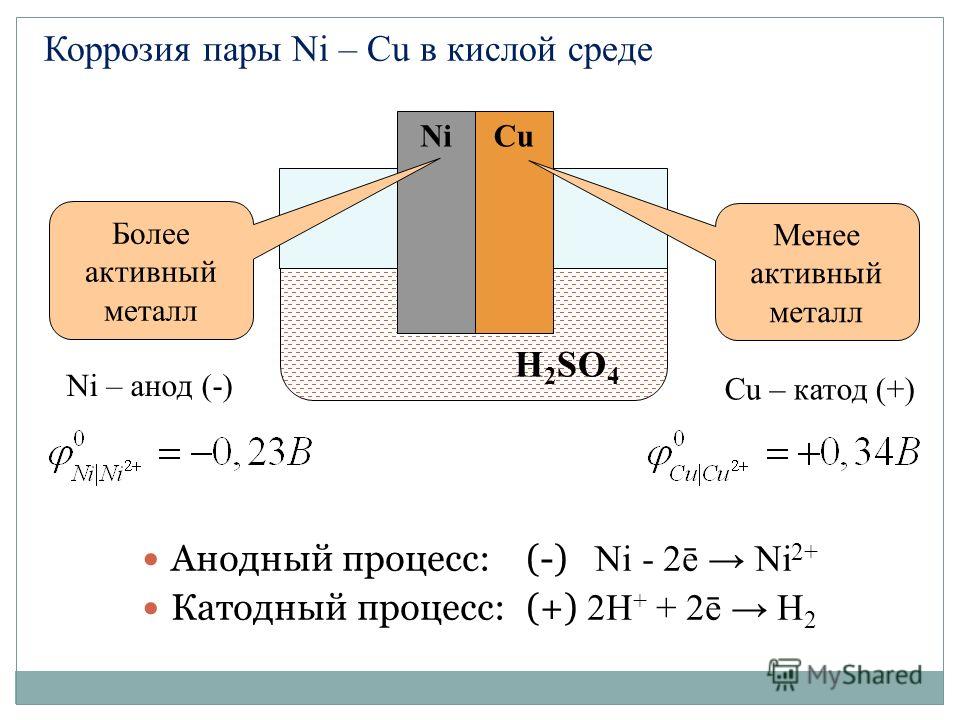 Остановить разрушение металла на 100% нельзя, однако способы защиты от контактной коррозии есть:
Остановить разрушение металла на 100% нельзя, однако способы защиты от контактной коррозии есть:
- Покрасить поверхность металлов в районе стыка.
- Нанесение совместимых покрытий из металла.
- Изоляция соединения от атмосферы.
- Электрическая изоляция места соединения.
- Установка неметаллических прокладок, шайб в болтовых соединениях.
Важно!
На скорость гальванической коррозии влияет площадь поверхности анода и катода. Если большой анод соединить с маленьким анодом, то он будет ржаветь медленнее. У зависимости есть и обратный эффект. Например, болты из нержавейки используйте для крепления алюминия, а не наоборот.
Неправильная компоновка контактных пар – это путь к выходу из строя узлов креплений в трубопроводах или металлоконструкциях.
Оцените нашу статью
[Всего голосов: 4 Рейтинг статьи: 4]
Гальванические пары металлов
Задать вопрос
раздел статьи
оглавление
контакты
Обучение и техническая поддержка для проектировщика на Prof-il.
Вы здесь:
оглавление//
гальванические пары металлов
Гальванические пары металлов
Атмосферная коррозионная стойкость алюминия обьясняется наличием оксидной пленки, образующейся сразу после взаимодействия металла с кислородом воздуха (Литер.: В.Ф. Хенли «Анодное оксидирование алюминия и его сплавов»).
Табл. 1 Совместимость металлов и сплавов
С — совместимые
Н — несовместимые
П — совместимые при пайке, но несовместимые при непосредственном соприкосновении, так как образуют гальваническую пару
ПОС — припой оловянно-свинцовый
Сталь — нелегированная
Пример нежелательных гальванических пар:
1 ПАРА: алюминий и все сплавы на его основе не рекомендуется и недопустимо сочетать:
— с медью и ее сплавами
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
— с оловом
— с никелем
— с хромом
2 ПАРА: алюминий и все сплавы на его основе не рекомендуется и недопустимо сочетать:
— с титаном и с его сплавами
3 ПАРА: магниево-алюминиевые сплавы не рекомендуется и недопустимо сочетать:
— с хромом
— со свинцом
— со сталью легированной и нелегированной
— с медью
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
— с оловом
— с никелем
4 ПАРА: цинк и его сплавы не рекомендуется и недопустимо сочетать:
— с медью и ее сплавами
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
5 ПАРА: никель и хром не рекомендуется и недопустимо сочетать:
— с медью и ее сплавами
— с серебром
— с золотом
— с платиной
— с палладием
— с родием
6 ПАРА: сталь нелегированная, олово, свинец, кадмий не рекомендуется и недопустимо сочетать:
— с серебром— с золотом
— с платиной
— с палладием
— с родием
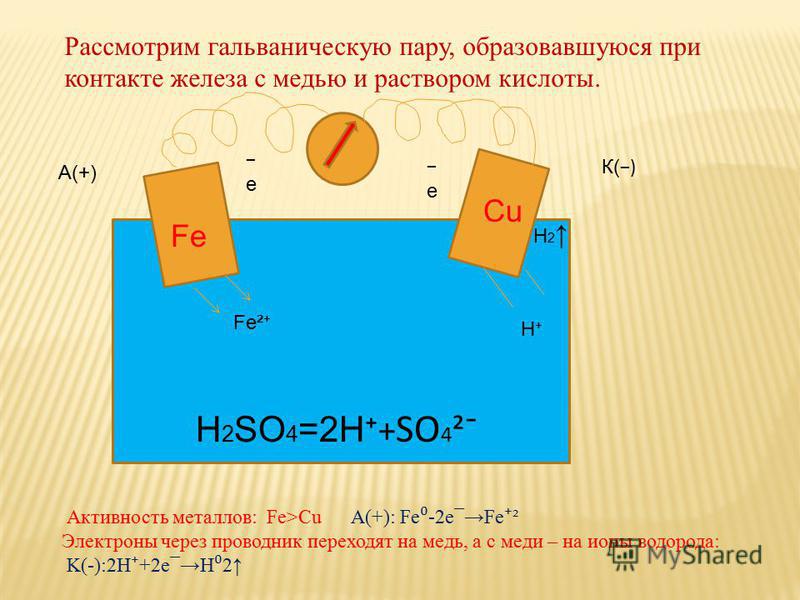
Рисунок 1 — Гальваническая коррозия двух деталей из разнородных металлов
Гальваническая коррозия более активного металла начинается в тот момент, когда две или более детали из разнородных металлов, имеющие взаимный контакт (благодаря обычному соприкосновению, или же посредством проводника) помещаются в электролит (любую жидкость, проводящую электричество).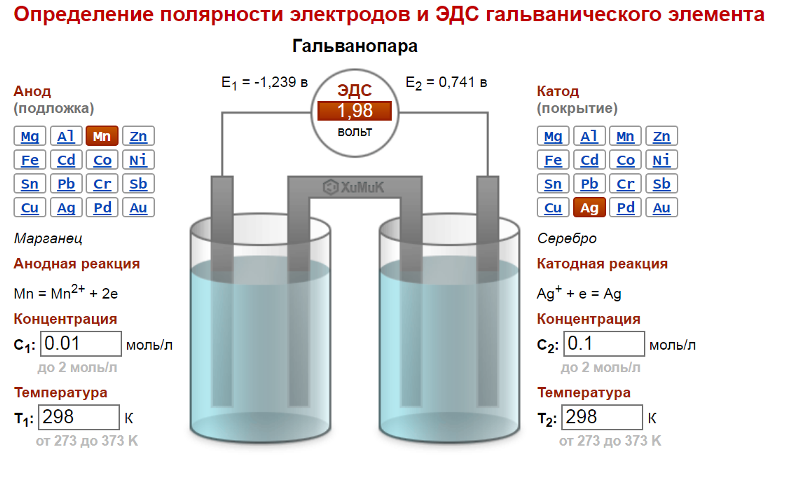 Электролитом может быть что угодно, за исключением химически чистой воды. Не только соленая морская, но и обычная вода из-под крана благодаря наличию минеральных веществ является превосходным электролитом, и с ростом температуры электропроводность ее только растет.
Электролитом может быть что угодно, за исключением химически чистой воды. Не только соленая морская, но и обычная вода из-под крана благодаря наличию минеральных веществ является превосходным электролитом, и с ростом температуры электропроводность ее только растет.
Катод — электрод, на котором происходит процесс восстановления, а анод — это электрод, где протекают окислительные процессы.
Ряд активности металлов (электрохимический ряд напряжений металлов)
1 — Активные металлы
2 — Металлы средней активности
3 — Неактивные металлы
Химическая коррозия — металлы защищают себя оксидной пленкой на своей поверхности, является ли она самовосстанавливающейся, вот вопрос, как в случае алюминия, нержавеющей стали, цветных металлов или же как у стали отделяется.
Рис 2 — многослойная панель на основе сотового или гофро алюминия «Perfaten»
Рис 3 — угловое соединение многослойной панели
Статья «Алюминиевая кассета», ссылка
Рис 4 — структура многослойной панели
Размеры: H= от 6 до 50мм. наверх
наверх
При копировании материалов проекта обязательно ставить активную ссылку на страницу источник: http://prof-il.ru
. Гальваническая совместимость алюминия и меди.
—— доб.
этот текст заменяется на bannerText
В. Я реставрирую винтажный туристический трейлер Airstream. Он имеет внутреннюю (и внешнюю) алюминиевую кожу. Я думаю об установке деревянных панелей поверх внутренней обшивки и использовании медных заклепок (строго для эстетики) для крепления панелей к алюминиевой обшивке. Влажность салона сильно снижена, но это реальная возможность.
Приведет ли использование медных заклепок в данном случае к значительному износу алюминиевой обшивки?
Стив Адамс
Любитель — Анкоридж, Аляска
2 апреля 2023
Черные алюминиевые заклепки
Доп. Ссылка
Ваши покупки делают отделку.com возможной
А. Привет, Стив. Продаются заклепки с медными головками и алюминиевыми сердечниками, поэтому некоторые продавцы считают, что это нормально, а место установки относительно не подвержено коррозии, поэтому вы, безусловно, можете рискнуть.
С другой стороны, хуже гальванической пары, чем медь и алюминий, по сути нет, и я бы на ее месте искал цельноалюминиевые заклепки медного цвета, а если бы не нашел, то мог бы и поговорить сам в черный 🙂 С уважением и удачей,
Тед Муни, P.E. RET
Стремление жить Алоха
Finishing.com — Пайн-Бич, Нью-Джерси
Тесно связанные исторические посты, сначала самые старые …
В. Мы хотели бы знать гальванический эффект, когда у нас есть болтовое соединение Алюминий -медь, может есть таблица опыта или данные расчетных значений.
Спасибо за помощь.
Gonzalo Ramirez
— Мехико, Мексика
2001
A. Алюминий будет очень восприимчив к гальванической коррозии при контакте с медью, если предположить, что эти два металла также находятся в контакте с общим электролитом (например, водой с некоторым содержанием ионов). Почти в любом учебнике или справочнике по коррозии есть таблица гальванического ряда. Чем дальше друг от друга расположены два металла или сплава на столе, тем быстрее будет коррозия менее благородного из двух, когда они соприкасаются.
Чем дальше друг от друга расположены два металла или сплава на столе, тем быстрее будет коррозия менее благородного из двух, когда они соприкасаются.
Larry Hanke
Minneapolis, Minnesota
A. Дополнительное примечание: залужите медные болты или другие медные детали, это поможет остановить или замедлить гальваническую атаку.
Крис Снайдер
, гальванопластика — Шарлотта, Северная Каролина
A. Также позаботьтесь о том, чтобы на медную шину было нанесено заводское серебряное покрытие. Это улучшит болтовые соединения за счет снижения сопротивления и предотвратит коррозию. Кроме того, поскольку он превращает красновато-черную медь в красивый равномерный серый цвет, он прекрасно сочетается с естественным цветом алюминия. Покрытия «Silver Flash» очень тонкие, поэтому дополнительные затраты составляют всего лишь несколько копеек в расчете на фут по сравнению с обычными шинами.
В. Карл Эриксон
Карл Эриксон
— Рим, Нью-Йорк
В. Я также думаю о соединении меди и алюминия, на этот раз в антенной установке. Каждый комментарий выше я могу понять и понять, пока У. Карл Эриксон не о серебре.
Единственные гальванические таблицы, которые я могу найти, относятся к коррозии в морской воде, но они все же ранжируют металлы от наиболее анодных до наиболее катодных. Например: www.eaa1000.av.org/technicl/corrosion/galvanic.htm
На этой странице автор перечисляет некоторые правила проектирования, в том числе необходимость иметь низкое отношение C/A (следствие IV). Следовательно, олово/алюминий лучше, чем медь/алюминий. Но серебро находится в дальнем конце катодного спектра, и по этой логике соединение серебро/алюминий очень нежелательно. Другие источники говорят, что серебро/золото/графит очень благородны. Что это значит для коррозии бедных маленьких анодов?
Кроме того, электрическая проводимость для меня необязательна. Что лучше: конформное покрытие медной платы или анодирование алюминиевой части?
Марк Нельсон
— Мельбурн, Флорида
2001
A. Перейдите по этой ссылке www.corrosionsource.com/handbook/galv_series.htm, чтобы ознакомиться с серией гальванических материалов. При использовании стандартного водородного электрода разница между медью и алюминием составляет -0,50 В.
Перейдите по этой ссылке www.corrosionsource.com/handbook/galv_series.htm, чтобы ознакомиться с серией гальванических материалов. При использовании стандартного водородного электрода разница между медью и алюминием составляет -0,50 В.
Несмотря на все ответы здесь. Коррозия алюминия/меди довольно сложна. Почему? Поскольку алюминий имеет оксид на поверхности, стабильность оксида определяет его характеристики. Гальванический ряд не всегда предсказывает реакцию в абсолютном выражении, поскольку нам нужно будет учитывать площадь двух металлов. Хлорид и медь могут вызвать точечную коррозию алюминия. Наконец, таблица скорости коррозии зависит от области. В Мексике уровень загрязнения самый высокий в мире. SO4, CO2, Cl-, F-2 легко образуют кислоты с влагой и вызывают коррозию. Атмосферная коррозия варьируется от места к месту.
Кам Дианатха
— Даллас, Техас
2004
В. Привет! Меня интересует эта тема, так как я собираюсь соединить медную трубу с алюминиевой частью (резьбовое соединение, ниппель на алюминии с крокс-гайкой для медной трубы или аналогичный). Вода, протекающая через систему, является чистой (питьевой). Есть ли проблема с этим суставом? Поможет ли мне вставить между ними отрезок трубы из ПВХ?
Вода, протекающая через систему, является чистой (питьевой). Есть ли проблема с этим суставом? Поможет ли мне вставить между ними отрезок трубы из ПВХ?
Все змеевики теплопередачи по всему миру изготовлены с алюминиевым оребрением, механически закрепленным на медной трубе, и все они очень хорошо работают в течение многих лет на крышах и в различных средах, без коррозии. Как они не ржавеют?
Крис Моана
— Окленд, Новая Зеландия
22 июня 2010 г.
В. Я думал о сборке солнечного коллектора, используя инструкцию на сайте www.n3fjp.com/solar, но меня беспокоят медные трубки с алюминиевыми защелками на поглотителях. будет настраивать систему на преждевременный отказ? Или это маловероятно, поскольку между этими разнородными металлами не будет проходить жидкости?
Надеюсь получить ответ от кого-то, кто знает об этом.
Спасибо,
Кеннет Форрестер
— Ричмонд, Вирджиния, США
19 ноября 2012 г.
В. Могут ли другие разнородные металлы притягиваться к области гальванической коррозии при наличии гальванической коррозии? Пример: когда алюминий и медь образуют узел гальванической коррозии, может ли растворимое железо попасть в этот узел?
Robert Aguirre
— Naperville, Illinois USA
1 марта 2013 г.
A. Привет, Роберт. Ваше понимание явления может быть глубже моего, и я могу неправильно понять вопрос, но я бы сказал «нет».
Начнем с одного металла, не связанного ни с каким другим металлом. Он состоит из атомов с положительно заряженными ядрами (хорошо, «ядрами», мисс Крабэппл), которые окружены электронами, уравновешивающими заряды, и все в порядке. Затем, допустим, эти атомы подвергаются воздействию коррозионной среды (похититель электронов). Агрессивная среда крадет электрон. Теперь этот атом больше не атом, а положительно заряженный ион в поисках электрона; поэтому он растворяется в среде в поисках электрона, чтобы уравновесить его. Итак, что на самом деле вызывает коррозию, так это потеря электронов из металла.
Итак, что на самом деле вызывает коррозию, так это потеря электронов из металла.
Металлы обладают электропроводностью, т. е. электроны могут перемещаться по ним из одного места в другое так же, как по проводу. Таким образом, если два разных металла каким-либо образом механически соединены без электрического изолятора между ними, электроны могут проходить через них.
Теперь возьмите кусок двух разных металлов, соединенных вместе, и подвергните их воздействию агрессивной среды, которая крадет электроны. Гальваническая защита/коррозия происходит следующим образом: когда у более благородного металла (в данном случае у меди) коррозионный раствор украл у него электрон, он имеет большее сродство к электронам, чем неблагородный металл, и немедленно крадет электрон у неблагородный металл (в данном случае алюминий). В результате атом меди остается уравновешенным атомом металла, а атом алюминия терпит неудачу и растворяется в растворе.
С уважением,
Тед Муни, ЧП
Стремление жить Алоха
Finishing. com — Пайн-Бич, Нью-Джерси
com — Пайн-Бич, Нью-Джерси
В. Подрядчик прикрепил короткие куски 25 мм меди к алюминиевым угловым стойкам, сплющив один конец и зафиксировав его цинковыми болтами. Посты были по ошибке обрезаны одним из его оперативников. Затем медь уйдет в подоконник/пол и будет заполнена бетоном.
Стоит ли волноваться? Сам алюминиево-медный стык закрывается клипсой из ПВХ и подвергается воздействию только ИРЛАНДСКОГО влажного воздуха.
Патрик Маллин
— Ома Тайрон Ирландия
14 мая 2013 г.
A. Цинковое покрытие на болтах исчезнет первым.
Khzem Vahaanwala
Saify Ind
Бангалор, штат Карнатака, Индия
A. Привет, Патрик. Фото мне бы точно помогло — извините, я заблудился 🙂
С уважением,
Тед Муни, ЧП
Стремление к жизни Aloha
Finishing.com — Пайн-Бич, Нью-Джерси
Совместимость медных заглушек с алюминиевыми вентиляционными трубами
В. Моя ассоциация домовладельцев очень строга и требует меди для мигания и других воздействий. У меня, очевидно, есть алюминиевые вентиляционные трубы для моей сушилки и вытяжки. Если я поставлю медные колпачки на эти трубы, навлеку ли я на себя неприятности или это имеет значение?
Моя ассоциация домовладельцев очень строга и требует меди для мигания и других воздействий. У меня, очевидно, есть алюминиевые вентиляционные трубы для моей сушилки и вытяжки. Если я поставлю медные колпачки на эти трубы, навлеку ли я на себя неприятности или это имеет значение?
Брайан Эллис
— Чесапик Вирджиния
12 мая 2014 г.
А. Привет, Брайан. Теоретически алюминий подвергается гальванической коррозии рядом с местом соединения с медью, когда он влажный. Но это не такое критическое применение, как в самолете, а дождевая вода не обладает высокой проводимостью. На практике я бы просто не беспокоился об этом.
С уважением,
Тед Муни, ЧП
Стремление жить Алоха
finish.com — Пайн-Бич, Нью-Джерси
В. У меня есть вопрос по этой теме. Мы изучаем использование меди в бытовых приборах. У меня есть толстая медная пластина (чистота 99,9%) и я ставлю на нее алюминиевую кастрюлю. Когда я нагрел пластину (газовое пламя ниже), мы получили чешуйчатое черное окисление на поверхности меди, где соприкасались два металла. Также потребовалось больше времени для закипания воды (по сравнению с обычной чугунной плитой). Однако медь должна иметь более высокую теплопроводность. Так как же он мог закипеть медленнее? Мы думаем, что между ними возникла гальваническая реакция, а черное окисление действовало как изолятор и замедляло передачу тепла. Это звучит правдоподобно? Можем ли мы нанести на медь покрытие или гальванопокрытие, чтобы предотвратить образование этого слоя окисления? Многие кастрюли и сковороды изготовлены из алюминия или анодированного алюминия, поэтому просто использование кастрюль из нержавеющей стали — недостаточно хорошее решение.
Когда я нагрел пластину (газовое пламя ниже), мы получили чешуйчатое черное окисление на поверхности меди, где соприкасались два металла. Также потребовалось больше времени для закипания воды (по сравнению с обычной чугунной плитой). Однако медь должна иметь более высокую теплопроводность. Так как же он мог закипеть медленнее? Мы думаем, что между ними возникла гальваническая реакция, а черное окисление действовало как изолятор и замедляло передачу тепла. Это звучит правдоподобно? Можем ли мы нанести на медь покрытие или гальванопокрытие, чтобы предотвратить образование этого слоя окисления? Многие кастрюли и сковороды изготовлены из алюминия или анодированного алюминия, поэтому просто использование кастрюль из нержавеющей стали — недостаточно хорошее решение.
Ханс Венцель
— Фуллертон, Калифорния, США
16 июня 2014 г.
A. Привет, Ханс. Нет, мне это не кажется правдоподобным. Гальваническая коррозия включает два электрических пути: металлический путь, по которому могут течь электроны, и ионный путь (жидкость), по которому могут течь ионы. Если одного пути не существует (в данном случае жидкостного пути), я не думаю, что у вас может быть гальваническая коррозия.
Если одного пути не существует (в данном случае жидкостного пути), я не думаю, что у вас может быть гальваническая коррозия.
Гальваническая коррозия, конечно, не единственный возможный вид коррозии.
С уважением,
Тед Муни, ЧП
Стремление жить Алоха
finish.com — Пайн-Бич, Нью-Джерси
В. Меня интересует эта тема, потому что я буду подключать две батарейки АА через перемычку из алюминиевой фольги (алюминиевой проводящей ленты 3M) — Как вы думаете, может ли в связи с этим возникнуть гальваническая коррозия? Будет всего 3 вольта.
Буду признателен за помощь
Карлос Вильянуэва
— Чиуауа, Мексика
12 августа 2014 г.
А. Привет, Карлос. Гальваническая коррозия обычно не является проблемой в благоприятной среде, в которой обычно находятся электронные устройства. Я не совсем знаком с этой проводящей лентой, но я считаю, что клей является проводящим, поскольку голый алюминий не будет должным образом служить контактной поверхностью.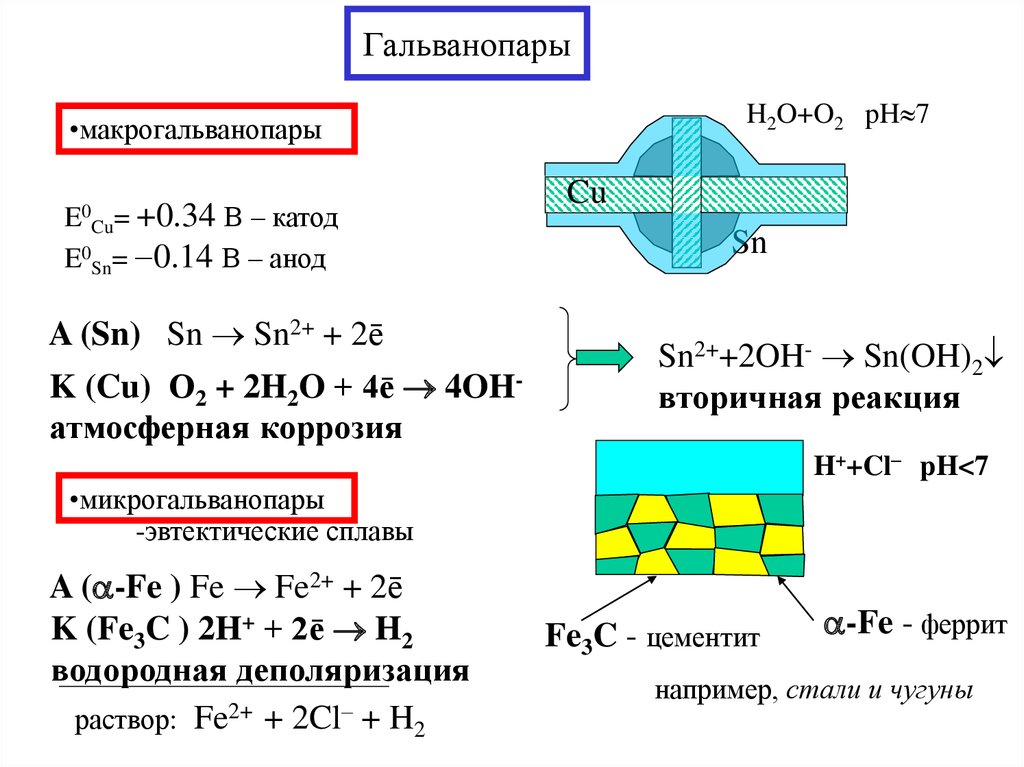 этот тип. Что происходит, когда батареи необходимо заменить, если один их конец заклеен скотчем? (Я думаю, что контакты на обоих концах батарей должны быть никелевыми или химически никелированными, а не алюминиевой лентой).
этот тип. Что происходит, когда батареи необходимо заменить, если один их конец заклеен скотчем? (Я думаю, что контакты на обоих концах батарей должны быть никелевыми или химически никелированными, а не алюминиевой лентой).
С уважением,
Тед Муни, ЧП
Стремление жить Алоха
Finishing.com — Пайн-Бич, Нью-Джерси
В. Я строю аппарат для точечной сварки и думаю об использовании алюминиевых стержней для удерживания медных электродов. Очевидно, у этого есть потенциал для гальванической реакции, но он останется в моем гараже и не промокнет. Будет ли проблемой медленная гальваническая реакция? Повлияет ли это на проводимость медно-алюминиевого перехода? Я буду пропускать через него ток около 1000 ампер, поэтому важна хорошая проводимость.
Ли Рэтлифф
— МакКинни, Техас, США
15 августа 2014 г.
Соединение «No-Ox-Id»
Доп. Ссылка
Ваши покупки делают отделку. com возможной
com возможной
А. Привет, Ли. Возможно, вы правы в том, что гальваническая коррозия сама по себе не будет проблемой в сухой среде, но поверхность алюминия окисляется до пленки с высоким сопротивлением, и по этой причине алюминий без покрытия редко является удовлетворительным проводником. Если соединение собрано с компаундом «No-Ox-Id», то, вероятно, все будет в порядке.
С уважением,
Тед Муни, ЧП
Стремление жить Алоха
Finishing.com — Пайн-Бич, Нью-Джерси
В. Кажется, это противоречит гальванической коррозии, но если я поставлю кастрюлю Cu в посудомоечную машину со столовыми приборами из нержавеющей стали, все будет хорошо, но если я включите алюминиевую кастрюлю, медь выходит черной. Вы можете это объяснить?
Дэвид Денли
— Хьюстон, Техас, США
10 декабря 2014 г.
A. Привет, Дэвид. Я не уверен, что понимаю то, что вы описываете, но для гальванического воздействия требуется проводящая металлическая дорожка между двумя металлами. Если алюминиевая кастрюля не касается медной кастрюли и не касается столовых приборов, то гальванической коррозии не происходит. Если два из этих трех металлов соприкасаются, а не третий, то между ними может происходить гальваническое воздействие, но не между третьим.
Если алюминиевая кастрюля не касается медной кастрюли и не касается столовых приборов, то гальванической коррозии не происходит. Если два из этих трех металлов соприкасаются, а не третий, то между ними может происходить гальваническое воздействие, но не между третьим.
Алюминиевые кастрюли нельзя мыть в посудомоечной машине. Обычные моющие средства сильно щелочны и легко разрушают алюминий.
С уважением,
Тед Муни, ЧП
Стремление жить Алоха
finish.com — Пайн-Бич, Нью-Джерси
В. Здравствуйте. Я хотел бы поставить солнечный медный «ионизатор» в джакузи на кедровых дровах. Я не хочу добавлять в воду химические вещества, такие как бром, хлор и т. д., которые будут меняться примерно раз в неделю. «Плита» представляет собой алюминиевый ящик, погруженный в пресную воду. Металлы не будут находиться в непосредственном контакте. Должен ли я беспокоиться о повреждении моей печи? Будет ли размещение жертвенного цинкового болта защищать алюминий? Спасибо!
Брюс Бэрд
— Уотертаун, Нью-Йорк, США
28 апреля 2015 г.
A. Привет, Брюс. Не может быть гальванической коррозии, если детали не соприкасаются, но это не обязательно означает, что медь и алюминий могут полностью противостоять коррозии. Цинковые аноды не защитят алюминий в пресной воде — вам понадобятся магниевые аноды.
Хотя я не совсем знаком с медными «ионизаторами», похоже, что они предназначены для добавления ионов меди в воду. Эта медь будет пытаться нанести покрытие на алюминий, и это может быть проблемой (я знаю, что медная пыль очень разъедает алюминий), но, надеюсь, магниевый анод защитит ее. Удачи.
С уважением,
Тед Муни, ЧП RET
Стремление жить Алоха
Finishing.com — Пайн-Бич, Нью-Джерси
В. Я ничего не знаю обо всех технических вещах, которые публикуют люди, но я надеюсь узнать, не будет ли это проблемой чтобы установить мои новые защитные ограждения желобов, сделанные из «алюминиевого проката», наши наши медные желоба. У них также есть сетка из нержавеющей стали, но не думаю, что она будет соприкасаться.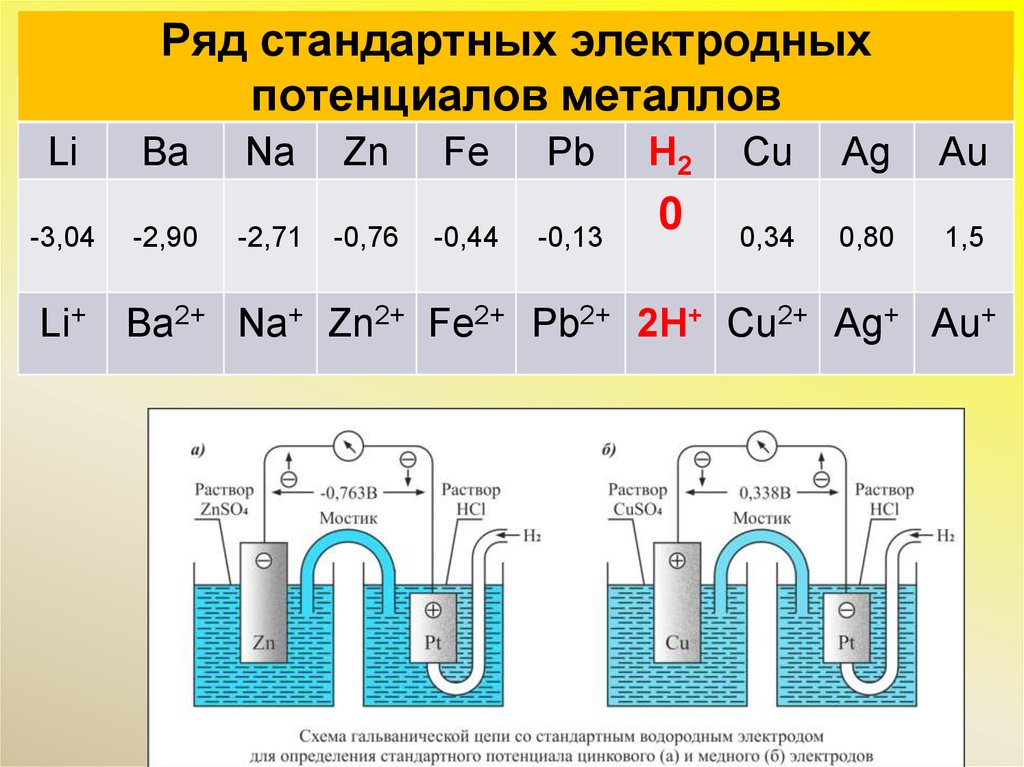 Компания сказала, что я могу нанести покрытие на алюминий, но это звучит как много дополнительной работы.
Компания сказала, что я могу нанести покрытие на алюминий, но это звучит как много дополнительной работы.
спасибо!!
Лулу Кукуэль
— Санта-Крус, Калифорния, США
13 ноября 2015 г.
А. Привет, Лулу. Предполагая, что вы не посыпаете крышу солью, не распыляете на нее средство от плесени или что-то еще, так что единственная влага — это дождевая вода, я сомневаюсь, что это будет проблемой. Гальваническая коррозия требует проводящей жидкости, а дождевая вода довольно непроводящая. Кроме того, защита водосточных желобов не является критически важным приложением.
С уважением,
Тед Муни, ЧП RET
Стремление жить Алоха
Finishing.com — Пайн-Бич, Нью-Джерси
В. Здравствуйте,
Я изучаю последствия гальванической коррозии из-за медной стружки и пыли, проникающих в алюминиевые катушки из-за высоких давлений при механической обработке. Я пытаюсь найти экономичные способы удаления медной пыли из машины (стали) перед введением алюминия.
Если это неприемлемое решение, не лучше ли покрыть алюминий защитным металлом, чтобы предотвратить появление точечных отверстий в катушке? Сильно ли это повлияет на теплопередачу змеевика? Если нет, то каким металлом посоветуете его покрыть?
Спасибо!
Ник
Ник Скотт
— Гренада, Миссисипи, США
2 декабря 2015 г.
А. Привет. Я не очень понимаю, что вы подразумеваете под «катушками» или о каком теплообмене вы говорите. Не допускать пыли, вероятно, лучшее решение, но вы можете покрыть катушки медью или никелем или даже покрыть их никелированием химическим способом.
С уважением,
Тед Муни, ЧП RET
Стремление жить Алоха
finish.com — Пайн-Бич, Нью-Джерси
Гальванизированные гвозди для каркаса и медный сайдинг
В. Здравствуйте, весь мой дом облицован медью с переплетением листов 4×2. Мы строим пристройку, и вместо того, чтобы удалять медь, подрядчик прибил каркас прямо к медным листам с помощью горячеоцинкованных гвоздей. Нужно ли мне беспокоиться о коррозии и поломке моего дополнения? Это такая масса меди вокруг обрамляющих гвоздей, что я не был уверен, как я к этому отношусь. Я вижу этот горячий гальв. в основном сталь с цинковым покрытием. Дайте мне знать, если фотография дома поможет
Нужно ли мне беспокоиться о коррозии и поломке моего дополнения? Это такая масса меди вокруг обрамляющих гвоздей, что я не был уверен, как я к этому отношусь. Я вижу этот горячий гальв. в основном сталь с цинковым покрытием. Дайте мне знать, если фотография дома поможет
Бриттани Келли
— Рок-Хилл, Южная Каролина
8 сентября 2016 г.
A. Привет, Бриттани. Как домовладелец, я не ожидал, что удаление сайдинга займет много времени; и медный сайдинг имеет хорошую стоимость лома. Так что мне кажется немного странным оставить старый медный сайдинг на месте, а не снимать его. Но я не строитель, и я полагаю, что, возможно, он не счел практичным прикреплять теперь свободный конец сайдинга к дому, если он обрежет его вместо того, чтобы просто оставить прикрепленными целые листы.
Гальваническая коррозия является проблемой во влажной среде, поэтому, если бы вы сказали мне, что он разрезал листы и прибил края оцинкованными гвоздями, я бы, вероятно, ожидал сильного окрашивания шляпок гвоздей. Но в том, что теперь будет сухой внутренний каркас, я не думаю, что ожидаю коррозии гвоздей.
Но в том, что теперь будет сухой внутренний каркас, я не думаю, что ожидаю коррозии гвоздей.
С уважением,
Тед Муни, ЧП RET
Стремление жить Алоха
finish.com — Пайн-Бич, Нью-Джерси
(Вы находитесь на 1-й странице этой темы) Следующая страница >
(Здесь нет «мертвых тем»! Ваш вопрос, ответ или комментарий вернут тему на горячую линию)
Вопрос, ответ или комментарий в ЭТОЙ теме -или- Начать НОВУЮ тему
Отказ от ответственности. С помощью этих страниц невозможно полностью диагностировать проблему отделки или опасность операции. Вся представленная информация предназначена для общего ознакомления и не является профессиональным мнением или политикой работодателя автора. Интернет в значительной степени анонимен и непроверен; некоторые имена могут быть вымышленными, а некоторые рекомендации могут быть вредными.
Если вы ищете продукт или услугу, связанную с отделкой металлов, проверьте следующие каталоги:
О нас/Контакты — Политика конфиденциальности — Следует подчеркнуть, что стойкость алюминия и алюминиевых сплавов к нормальным условиям окружающей среды очень высока. Основным источником защиты от коррозии является прочная самовосстанавливающаяся оксидная пленка, которая всегда присутствует на алюминии в атмосфере окружающего воздуха (рис. 1).
Основным источником защиты от коррозии является прочная самовосстанавливающаяся оксидная пленка, которая всегда присутствует на алюминии в атмосфере окружающего воздуха (рис. 1).
Рисунок 1 – Естественная защита алюминия от коррозии – поверхностная оксидная пленка [4]
Основные виды коррозии алюминия
Для коррозии алюминия характерны следующие основные виды [4]:
- общая коррозия
- щелевая коррозия
- Фреттиниг-коррозия
- Коррозия под напряжением
- Гальваническая коррозия
- Питтинговая (точечная) коррозия
- межкристаллитная коррозия
- подповерхностная коррозия
Рисунок 2 – Общая коррозия алюминия: растворение естественной оксидной пленки
растворами сильных щелочей и некоторых кислот [4]
Рисунок 3 – Щелевая коррозия алюминия [4]
Рисунок 4 – Фреттинг-коррозия алюминия алюминий: взаимное трение двух алюминиевых компонентов
в условиях шероховатого контакта [4]
] 9Рис.
под воздействием ионов хлора [4]
Рисунок 8 – Межкристаллитная коррозия и подповерхностная коррозия [4]
В зависимости от условий окружающей среды, нагрузки и функциональности детали любого из видов коррозии могут привести к преждевременному выходу из строя. Более того, неправильная эксплуатация алюминиевых деталей и изделий может усугубить коррозионные процессы.
Гальваническая коррозия алюминия
Наиболее частые ошибки проектирования алюминиевых конструкций связаны с гальванической коррозией. Гальваническая или электрохимическая коррозия возникает, когда два разнородных металла образуют электрическую цепь, замыкаемую жидким электролитом или пленкой, или агрессивной средой. В этих условиях разность потенциалов между разнородными металлами создает электрический ток, проходящий через электролит, который (ток) приводит к коррозии в первую очередь анода или менее благородного металла из этой пары.
РЕЗЮМЕ гальваническая коррозия
Когда два разных металла вступают в непосредственный контакт с электропроводящей жидкостью, опыт показывает, что один из них может подвергаться коррозии, т.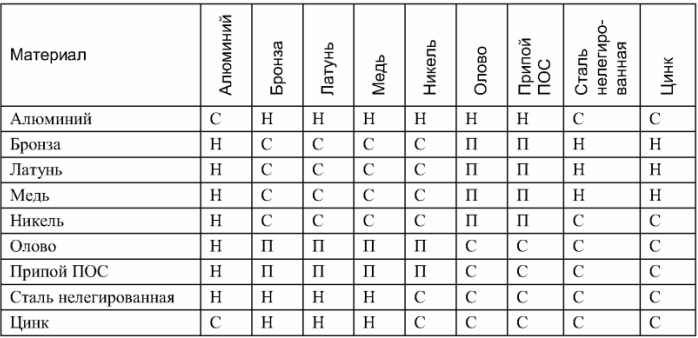 е. подвергаться коррозии. Это называется гальванической коррозией.
е. подвергаться коррозии. Это называется гальванической коррозией.
Другой металл не подвергается коррозии, наоборот, он будет защищен от этого вида коррозии.
Этот вид коррозии отличается от видов коррозии, которые могли бы возникнуть, если бы оба этих металла были помещены по отдельности в одну и ту же жидкость. Гальваническая коррозия может возникнуть с любым металлом, как только два разных металла соприкасаются в электропроводящей жидкости.
Внешний вид гальванической коррозии
Внешний вид гальванической коррозии очень характерен. При этом коррозия не разлетается по всей поверхности изделия, как в случае с точечной — питтинговой — коррозией. Гальваническая коррозия локализуется в зоне плотного контакта алюминия с другим металлом. Коррозионное воздействие на алюминий имеет равномерный характер, оно развивается в глубине кратеров, имеющих более или менее округлую форму [3 [.
Все алюминиевые сплавы одинаково подвержены гальванической коррозии [3].
принцип батареи
Гальваническая коррозия работает как батарея, которая состоит из двух электродов:
- катод, где идет реакция восстановления Анод
- , где протекает реакция окисления.
Эти два электрода погружены в проводящую жидкость, называемую электролитом. Электролит — это обычно разбавленный раствор кислоты, например, серной кислоты, или солевой раствор, например, медный купорос. Эти два электрода подключены к внешней электрической цепи, по которой циркулируют электроны. Внутри жидкости перенос происходит электрическим током, движутся ионы. Жидкость, таким образом, обеспечивает ионное электрическое соединение (рис. 9).).
Рисунок 9 – Принцип действия гальванического элемента [3]
На рисунке 1 показан элемент, в котором электролитом является раствор серной кислоты. Серная кислота полностью диссоциирует в воде (поскольку это сильная кислота) с образованием ионов Н + , определяющих кислотность среды. Происходит следующая электрохимическая реакция [3]:
Происходит следующая электрохимическая реакция [3]:
- цинковый анод окисляется:
Zn → Zn 2+ + 2e −
на медном катоде восстановлены протоны H + :
2N + + 2E — → N 2
Полная реакция:
Zn + H 2 O → ZN (OH) 2 2 O → Zn (OH) 2 + H + H + 2 . Этот элемент производит электричество за счет потребления цинка, который выделяется в виде гидроксида цинка Zn (OH) 2 . Для работы элемента необходимо одновременное выполнение трех условий: Если хотя бы одно из этих условий не выполнено, например, при нарушении электрического контакта, то ячейка не будет вырабатывать электричество, и окисления на аноде (как и восстановления на катоде) не произойдет. Гальваническая коррозия основана на том же принципе, и для ее возникновения необходимо одновременное выполнение следующих трех условий [3]: Для всех металлов, которые относятся к различным типам, возможна гальваническая коррозия. Металл с электроотрицательным потенциалом (или более электроотрицательный металл, если они оба электроотрицательны) действует как анод. Склонность различных металлов к образованию гальванических паров и направленность электрохимического действия в различных агрессивных средах (морская вода, тропический климат, промышленная атмосфера и др.) показаны в так называемом гальваническом ряду. Чем дальше друг от друга удалены металлы в этих рядах, тем серьезнее может быть гальваническая коррозия. В разных агрессивных средах эти последовательности металлов могут быть разными (рис. Место контакта необходимо смачивать водным раствором, для обеспечения ионной проводимости. В противном случае нет возможности для гальванической коррозии. Электрический контакт между металлами может иметь место либо при непосредственном контакте двух металлов, либо с помощью крепежных деталей, например, болта. Рисунок 10 [1] Как видно из рисунка схемы 10 алюминий и его сплавы становятся анодами в электрохимических элементах с большинством металлов, а алюминий корродирует, как говорится, жертвенно защищая от коррозии металл и другие гальванические пары. Только магний и цинк, в том числе из оцинкованной стали, Они более анодны и поэтому, сами подвергаясь коррозии, защищают от нее алюминий. Алюминий и кадмий вообще имеют почти одинаковые электродные потенциалы и при этом ни алюминий, ни кадмий не подвержены гальванической коррозии. К сожалению, кадмий оказался очень токсичным и используется все реже и реже, а во многих странах просто запрещен в качестве антикоррозионной защиты. Взаимное расположение двух металлов или сплавов в гальваническом ряду указывает только на возможность гальванической коррозии, если разница их электрохимических потенциалов достаточно велика. Больше эта цифра ни о чем не говорит, и особенно ничего — о скорости или интенсивности гальванической коррозии. Он может быть нулевым, незначительным или даже невидимым. Интенсивность его зависит от типов металлов, которые вступают в контакт — гальваническая пара. В строительстве алюминиевые детали, подверженные влиянию климата и погодных условий, могут быть соединены винтами из обычной стали. Опыт показывает, что алюминий при контакте со стальными болтами подвергается лишь очень поверхностной коррозии. Образующаяся ржавчина, не оказывающая никакого влияния на алюминий, полностью пропитывает слой оксида алюминия и образует пятно на поверхности. Собственно, для алюминиевых конструкций при контакте с оголенной сталью важно влияние на ее внешний вид и декоративные качества, а не способность сопротивляться коррозии. Это явление имеет следующее объяснение: Судя по гальваническому ряду, цинк более электроотрицателен, чем алюминий. Крепеж из оцинкованной стали может, таким образом, применяться для соединения и сборки конструкций из алюминиевых сплавов. Следует помнить, что когда цинковое покрытие слишком изнашивается, чтобы защитить сталь и алюминий, возникает предыдущий сценарий контакта между алюминием и голой сталью [3] . Хотя существует большая разность потенциалов между нержавеющей сталью и алюминиевыми сплавами – около 650 мВ, гальваническую коррозию на алюминии в контакте с нержавеющей сталью можно увидеть очень редко. Поэтому алюминиевые конструкции очень часто собирают с помощью болтов и винтов из нержавеющей стали [3]. Контакт между алюминиевыми сплавами и медью, а также медными сплавами (бронза, латунь) приводит к очень незначительной гальванической коррозии алюминия при воздействии атмосферных условий. Тем не менее, рекомендуется обеспечить электрическую изоляцию между двумя металлами, чтобы локализовать коррозию алюминия. Следует отметить, что продуктом коррозии меди является, т.н., раз a. Эта патина — голубовато-зеленый налет на меди, состоящий в основном из карбоната меди. Эта патина химически воздействует на алюминий и может быть уменьшена до образования мелких частиц меди. Эти частицы меди, в свою очередь, могут вызывать локальную точечную коррозию алюминия [3]. Ускоренная гальваническая коррозия обычно наиболее интенсивна вблизи стыков двух металлов; по мере удаления от стыка его интенсивность уменьшается. Существенное влияние на скорость коррозии оказывает величина отношения площади поверхности катода, контактирующего с электролитом, к площади открытой поверхности анода. Рисунок 11 [1] Рисунок 12 [1] Источники:
Условия гальванической коррозии
Различные типы металлов
 10).
10). Наличие электролита
Электрический контакт между металлами

гальванические пары
Пара: алюминий – нелегированная сталь

Пара: алюминий – Цинк Сталь
Пара: алюминий – нержавеющая сталь

Пара: алюминий – медь
Ближе к прикосновению – больше коррозии
 Желательно иметь малое отношение площади катода к площади анода.
Желательно иметь малое отношение площади катода к площади анода. Как избежать гальванической коррозии