Коррозия металлов. Виды и особенности. Защита и принцип действия
Коррозия металлов – это процесс разрушения металлической поверхности в результате неблагоприятного воздействия окружающей среды. Ее причиной является термодинамическая неустойчивость материала к влиянию различных веществ, которые с ним контактируют.
Разрушение поверхностей наступает вследствие химического или электрохимического взаимодействия неблагоприятной среды. Обе разновидности являются одинаково пагубными для изделий из металла.
Химическая коррозияДанный процесс осуществляется в среде, которая не производит передачу электрического тока. Он наблюдается, например, при нагреве, в результате чего осуществляется образование химических соединений, таких как сульфиды, а также различные виды пленок. Нередко образованные сплошные пленки становятся непроницаемыми и консервируют поверхность, поэтому последующая коррозия металлов останавливается. Такой защитный слой можно встретить на поверхности из алюминия, хрома, никеля и свинца. Пленка на стали или чугуне является непрочной, поэтому ее наличие не останавливает дальнейшее продвижение разрушения вглубь материала.
Пленка на стали или чугуне является непрочной, поэтому ее наличие не останавливает дальнейшее продвижение разрушения вглубь материала.
Химическая коррозия может быть двух видов:
- Газовой.
- Жидкостной.
Газовая возникает в результате действия агрессивной газовой среды или пара на поверхность металла, что сопровождается повышенными температурами. Благодаря горячей среде на поверхности отсутствует конденсат. В качестве газа может применяться кислород, диоксид серы, водяной пар, сероводород и так далее. Подобное коррозийное влияние может вызывать абсолютное разрушение активного металла, за исключением случаев, когда образуется защитная непроницаемая пленка.
Жидкостная коррозия металлов возникает в жидкостных средах, которые не способны передавать электричество. В первую очередь она наблюдается при контакте металлов с сырой нефтью, нефтепродуктами или смазочными маслами. При наличии в таких веществах небольшой доли воды, коррозия переходит в электрохимическую.
В обоих вариантах химической коррозии скорость разрушения является пропорциональной химической реакции, с которой окислитель проникает сквозь созданную оксидную пленку на поверхности.
Электрохимическая коррозия металловЭта разновидность разрушения поверхности металла происходит в среде, которая может передавать электрический ток. В результате данного процесса наблюдается изменение состава металла. Атомы удаляются от кристаллической решетки в результате анодного или катодного воздействия. При анодном влиянии ионы металла переходят в раствор жидкости, которая его окружает. При катодном влиянии получаемые при анодном процессе электроны связываются с окислителем. Наиболее распространенной является электрохимическая коррозия под воздействием водорода или кислорода.
Процесс влияния электрохимической коррозии на металлы зависит от уровня их активности. По данному критерию их разделяют на 4 группы:
- Активные.
- Средней активности.

- Малоактивные.
- Благородные.
Активные имеют высокую нестабильность. Для них характерно возникновение коррозии даже в нейтральной водной среде, которая лишена растворенного кислорода или окислителей. Ярким представителем такого металла является кадмий.
Металлы средней активности располагаются на таблице химических элементов между кадмием и водородом. Они неподвержены началу разрушения в нейтральной жидкостной среде лишенной кислорода, но начинают интенсивно поддаваться коррозии при влиянии кислот.
Малоактивные металлы располагаются в таблице Менделеева между водородом и родием. Они не подвергаются влиянию коррозии при контакте с нейтральными жидкостями и кислой средой. Для активизации процесса их разрушения необходимо наличие кислорода или прочих окислителей.
Благородные металлы отличаются стабильностью, благодаря чему подвержены коррозии только при воздействии кислой среды при условии контакта с сильными окислителями. К перечню благородных металлов относится платина, золото, палладий и иридий.
К перечню благородных металлов относится платина, золото, палладий и иридий.
Электрохимическая коррозия металлов является самой распространенной, поскольку естественные условия, в которых хранятся и эксплуатируются металлические изделия, зачастую подвержены влиянию влажной среды.
Различают следующие виды электрохимической коррозии:
- Электролитная – наблюдается при контакте с растворами солей, кислотами, оснований, в том числе и обычной водой.
- Атмосферная – наблюдается в условиях атмосферы, где содержатся испарения воды. Данный вид является самым распространенным, именно он влияет на практически все металлические изделия.
- Почвенная – наблюдается в результате воздействия влажной почвы, в составе которой могут содержаться различные химические элементы ускоряющие процесс разрушения металла. При воздействии с кислыми почвами процесс коррозии наблюдается наиболее агрессивно. Грунты с песком воздействуют медленней всего.

- Аэрационная – является более редкой и наблюдается в тех случаях, если к разным поверхностям металла оказывается неравномерный доступ воздуха. В результате неоднородного воздействия линии переходов между такими участками начинают разрушаться.
- Морская коррозия металлов подразумевает разрушение от влияния морской воды. Она выделяется в отдельную группу, поскольку данная жидкость отличается высоким содержанием солей и растворенных органических веществ. Это делает ее более агрессивной.
- Биокоррозия – данный вид разрушения возникает при условии воздействия на поверхность металла бактериями, которые в результате жизнедеятельности вырабатывают углекислый газ и прочие вещества.
- Электрокоррозия – такой вид разрушения металла наблюдается при воздействии на него блуждающих токов, что характерно для подземных сооружений, в частности рельсов метрополитена, стержней заземления, трамвайных линий и т.
 д.
д.
Голая поверхность подавляющего большинства металлов склонна к быстрой коррозии, поэтому для снижения разрушающего воздействия применяются различные способы защиты.
Покрытие изоляционными слоями:
- Другим металлом.
- Цементным раствором.
- Лаками.
- Красками.
- Битумом.
Одним из самых эффективных способов защиты от коррозии является покрытие поверхности одного металла другим, менее склонным к коррозии. Примером такого технического решения является оцинковка, когда сталь защищается слоем цинка. Внутренний металл полностью изолирован до тех пор, пока цинк в результате естественной коррозии, которая протекает очень медленно, полностью не разрушится, оголив сталь. Такой метод защиты является одним из самых эффективных, поскольку покрывной металл полотна удерживается на основании, поэтому его невозможно срывать слоями. Недостаток метода заключается в том, что при механическом воздействии можно сцарапывать тонкую защитную пленку.
Покрытие металла защитным цементным раствором, битумом, лаками и красками является также очень распространенным решением, которое все же уступает оцинковке. Это связано с неоднородностью составов основания и покрытия. В результате низкой адгезии краски готовое покрытие будет отслаиваться. Такая защита может покрываться трещинами, обеспечивая доступ влаги.
Коррозия металлов может быть приостановлена при наличии химического покрытия:
- Оксидирование.
- Фосфатирование.
- Азотирование.
- Воронение.
- Цементация.
Поверхность металла подвергается влиянию различных веществ, фосфатов, азота или оксидов, в результате чего создаются пленки, которые благодаря своей непроницаемости предотвращают разрушение. Такие методы применимы в первую очередь для сталей. Также распространенным решением является воронение стали, когда поверхность металла взаимодействует с органическими веществами. Обработанные таким способом поверхности приобретают темный цвет, напоминающий крыло ворона, за что данный метод и получил свое название. Одним из наиболее эффективных вариантов химического покрытия является цементация, когда на поверхность воздействуют углеродом, в результате чего создается корка вступившего в реакцию металла.
Одним из наиболее эффективных вариантов химического покрытия является цементация, когда на поверхность воздействуют углеродом, в результате чего создается корка вступившего в реакцию металла.
Для защиты от коррозии черных металлов может применяться технология изменения их состава. Добавление различных соединений позволяет получить сплавы, отличающиеся большей устойчивостью к коррозии. Примером такого соединения является нержавеющая сталь.
Самым необычным является протекторная защита, которая подразумевает покрытие сооружений из одного металла пластинами из более активного металла, так называемого протектора. Поскольку он имеет более отрицательный потенциал, то выступает в роли анода. Защищаемая поверхность используется как катод. Они соединяются между собой проводником тока, благодаря чему создаются неблагоприятные условия для протектора. Как следствие разрушению поддается именно он, в то время как ценное сооружение остается целым.
Более редким решение является изменение состав окружающей среды.
 В таких условиях коррозия металлов замедляется или не происходит. Данный метод подразумевает очистку состава жидкости или газа от кислот и солей, вызывающих разрушение. Такой метод применим далеко не во всех случаях, поскольку отличается техническими сложностями и определенной дороговизной. Его используют в разных механизмах. К примеру, могут применять в определенных средах только те металлы, для которых те не агрессивны.
В таких условиях коррозия металлов замедляется или не происходит. Данный метод подразумевает очистку состава жидкости или газа от кислот и солей, вызывающих разрушение. Такой метод применим далеко не во всех случаях, поскольку отличается техническими сложностями и определенной дороговизной. Его используют в разных механизмах. К примеру, могут применять в определенных средах только те металлы, для которых те не агрессивны.Похожие темы:
- Степень защиты IP. Маркировка. Выбор устройств
- Преобразователь ржавчины. Виды и работа. Применение
Типы и виды коррозий металла — Короли Воды и Пара на vc.ru
1245 просмотров
Коррозии металла
Сегодня мы с вами разберемся, узнаем многое про типы и виды коррозии металла. Изучим тему, узнав, откуда и из-за чего берётся коррозия на металле.
Откуда берётся, коррозия металла
Коррозия появляется из-за воздействия на него окружающей среды. Учёные выяснили, что это саморазрушение металлов и сплавов в ходе химических и физико-химических и электрохимических процессов. Так же есть практически аналогичный процесс, это разрушение металла методом физического воздействия, не надо его путать с коррозией, этот процесс называют: «эрозия» или же «износ».
Так же есть практически аналогичный процесс, это разрушение металла методом физического воздействия, не надо его путать с коррозией, этот процесс называют: «эрозия» или же «износ».
Также стоит сказать, что на появление ржавчины сильнее всего содействует влажная среда. На появление ржавчины, как и на все химические процессы, влияет температура окружающей среды, даже если температура воздуха будет различаться всего на 5-10 градусов, то разница в скорости уже будет видна. Таким образом, появляется ржавчина, она бывает разных видов и ниже мы расскажем именно про это.
Типы и виды коррозии
Коррозию в основном различают на четыре основных типа, а именно: электрохимическая, химическая, водородная и кислородная.
Электрохимическая коррозия
Электрохимической коррозией называют разрушение металла, вследствие взаимодействия с коррозионной средой гальванических элементов. Для появления электрохимической коррозии обязательна наличие электролита, с которыми будут соприкасаться электроды и другие элементы. Если процесс проходит в воде и в нем растворены соли, то процесс идет намного быстрее.
Если процесс проходит в воде и в нем растворены соли, то процесс идет намного быстрее.
Водородная и кислородная коррозия
Когда случается Восстановление ионов Н3О+ или же молекулы воды Н2О, это называют коррозией с водородной деполяризацией или же проще водородной коррозией. Такую коррозию чаще всего называют ржавчиной. Коррозия такого типа возникает во влажных местах либо же в водопроводных трубах (при скоплении конденсата). Каждый из нас видел коррозии такого типа, если не дома, то на улице уж точно.
Также коррозия может возникать, не только при прикосновении нескольких разных металлов. Элементы коррозии могут возникать и в случаи, если металл один. Если структура металла неоднородна, то она возникает также, так случается чаще ведь сейчас практически всегда в любом металле есть примеси в виде других металлов, это делается для экономии.
Химическая коррозия (при воздействии пара)
Химической коррозией считается ржавчина возникшая из-за касания и взаимодействия металла с средой которая полна активной коррозией, в отличии от электрохимической, процесс не идет совместно с электрохимическими реакциями и стоит на границе фаз.
- Газовая коррозия (при воздействии пара) – Это коррозия, которая возникает из-за взаимодействия с активными газами, которые находятся в среде, где находится, металл. Для хода газовой коррозии обязательна высокая температура среды. Такими газами могут быть: Кислород, пары воды, пары серы и другие.
- Жидкостная коррозия – Ржавчина этого типа может появится из-за соприкосновения с активными жидкостями, например нефть, керосин, бензин или почти со всеми маслами.
Защита от появления коррозии
Вы, наверное, задаетесь вопросом: «Если есть такое множество видов коррозии и если ржавчина может возникнуть практически везде, то мы не придумали как защитить металлы?» И это логичный вопрос, ведь люди постоянно придумывают, как облегчить свою жизнь. Наш ответ да, люди всё таки придумали, как защищать металлы от коррозии, и этих методов великое множество, ниже мы расскажем про нескольких из них.
Металлическое покрытие
Это самый простой метод защиты, металл, покрывают защитным слоем, другого уже заведомо обработанного металлом, уж простите за тавтологию. Таким тонким слоем можно защитить металл от возникновения ржавчины, таких покрытии есть великое множество, например анодное покрытие и катодное покрытие. К сожалению, покрытие такого типа не защищает от коррозии, которая возникает водородным методом, то есть от пара, от воды и так далее.
Химическое покрытие
Так же есть неметаллические покрытия для защиты металлов от ржавчины, химическое покрытие один из этих методов защиты, вот несколько из этих покрытий:
- Оксидирование;
- Фосфатирование;
- Азотирование;
- Воронение стали;
- Цементация.
Электрохимическая защита
В этом случае защита создаётся при помощи постоянного обеспечения током. Так же есть и другой метод электрохимической защиты, его называют Протекторной, при этой схеме К поверхности прицепляются другие куски металла уже обеспеченным защитой и это называют протектором.
Так же есть и другой метод электрохимической защиты, его называют Протекторной, при этой схеме К поверхности прицепляются другие куски металла уже обеспеченным защитой и это называют протектором.
Наши специалисты проконсультируют Вас и помогут в правильном подборе оборудования в паровые и пароконденсатные системы, во избежание появления коррозий.
Если у Вас остались вопросы, мы будем рады Вам помочь. С нами можно связаться любым удобным способом:
По почте: [email protected]
По телефону: +7 (343) 288-35-54 или WhatsApp
Подписывайтесь на наш Телеграм канал, там всегда много полезного и интересного.
Что вызывает коррозию?
Что такое коррозия?
Коррозия – это естественный процесс, связанный с износом металлических компонентов. Согласно NACE International , коррозия — это «разрушение вещества (обычно металла) или его свойств из-за реакции с окружающей средой». В конечном итоге это может привести к серьезному повреждению вашего здания или приложения и может стать очень дорогостоящим ремонтом.
Как возникает коррозия
Коррозия — это электрохимическая реакция, которая проявляется в нескольких формах, таких как химическая коррозия и атмосферная коррозия, последняя из которых является наиболее распространенной формой. Когда кислотные вещества (включая воду) вступают в контакт с металлами, такими как железо и/или сталь, начинает образовываться ржавчина. Ржавчина является результатом коррозии стали после того, как частицы железа (Fe) подверглись воздействию кислорода и влаги (например, влажности, пара, погружения). Когда сталь подвергается воздействию воды, частицы железа теряются в кислых электролитах воды. Затем частицы железа окисляются, что приводит к образованию Fe⁺⁺. Когда образуется Fe⁺⁺, два электрона высвобождаются и текут через сталь к другой области стали, известной как катодная область.
Кислород заставляет эти электроны подниматься вверх и образовывать гидроксильные ионы (ОН). Ионы гидроксила реагируют с FE⁺⁺ с образованием водного оксида железа (FeOH), более известного как ржавчина.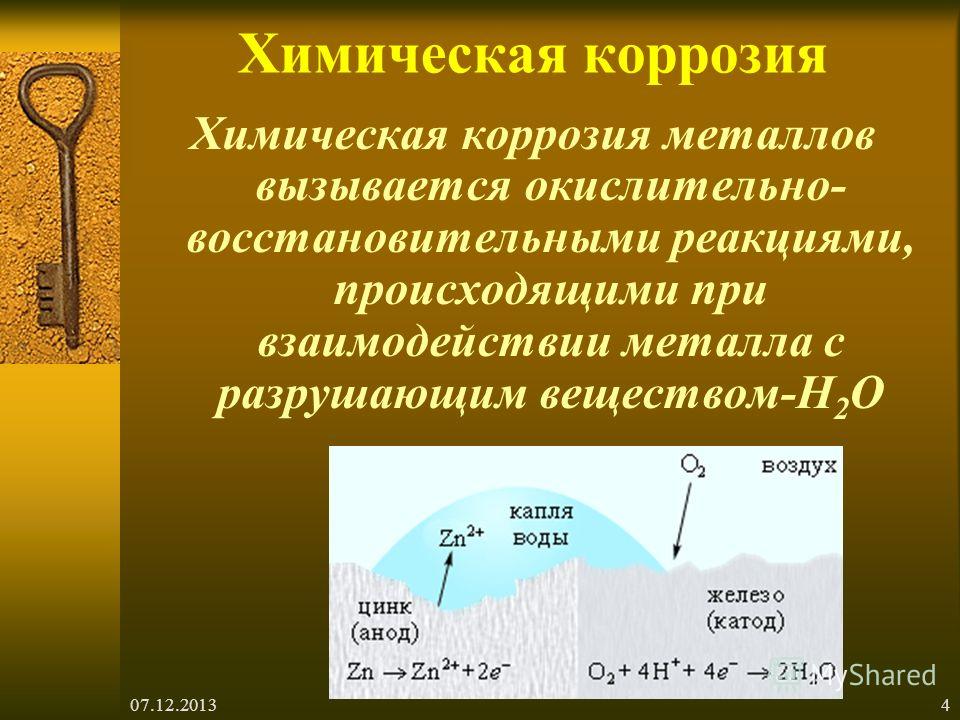 Там, где были пораженные частицы железа, теперь образовалась коррозионная ямка, а то место, где они сейчас находятся, называется продуктом коррозии (ржавчиной).
Там, где были пораженные частицы железа, теперь образовалась коррозионная ямка, а то место, где они сейчас находятся, называется продуктом коррозии (ржавчиной).
Коррозия может происходить с любой скоростью, в зависимости от среды, в которой находится металл. Однако, поскольку атмосферная коррозия широко распространена, рекомендуется принимать эффективные меры предосторожности, когда речь идет о предотвращении коррозии.
Удаление и обработка ржавчины
В зависимости от ситуации и применения вы можете обработать участок, подвергшийся коррозии. Если пораженный участок небольшой и поддается лечению, вам могут потребоваться некоторые инструменты и продукты для его удаления. Начните с удаления ржавчины с металла с помощью таких инструментов, как шлифовальный круг или игольчатый пистолет. Будьте осторожны, чтобы не нанести дополнительных повреждений металлу.
Для больших коррозионно-коррозионных участков может потребоваться постоянное защитное покрытие, такое как антикоррозионное защитное покрытие SI-COAT компании CSL. Вы также захотите потратить это время, чтобы посмотреть на приложение в целом на наличие других преждевременных признаков коррозии.
Вы также захотите потратить это время, чтобы посмотреть на приложение в целом на наличие других преждевременных признаков коррозии.
Как предотвратить коррозию?
Одним из лучших способов предотвращения коррозии является нанесение антикоррозионного защитного покрытия . Защитное покрытие защищает подложку, предотвращая контакт подложки с агрессивными средами (атмосферными, химическими и т. д.). Здесь, в CSL Silicones Inc, мы предлагаем два вида антикоррозионных защитных покрытий (один из них — экологически безопасный вариант с низким содержанием летучих органических соединений!), которые легко наносятся с помощью всего лишь одного слоя. Si-COAT® 579 AC защитное покрытие экономично и обеспечивает длительную защиту практически любой поверхности.
Покрытия экологически безопасны, обладают превосходной термостойкостью (могут выдерживать температуры от -76°F до 392°F), не мелеют и не выцветают, имеют малослойную пленку, требуют нанесения только одного слоя и имеют превосходная стойкость к УФ-излучению.
| |
|
Антикоррозионные защитные покрытия Si-COAT могут наноситься в самых разных областях, таких как конструкционная сталь, мосты, машины и оборудование, области с сильной коррозией, внешние поверхности резервуаров, металлические крыши, облицовка, и более.
Защитные покрытия Si-COAT AC идеально наносятся там, где необходима необходимая укрывистость и требуется максимальная защита, адгезия, эластичность и долговечность.
Если вас интересует защита от коррозии, посетите нашу страницу «Антикоррозионные защитные покрытия » для получения дополнительной информации.
Опубликовано в понедельник, 12 сентября 2016 г. в Блог
Какие металлы ржавеют? | Железо и медь ржавеют?
Что такое ржавчина?
Ржавчина, обычно называемая окислением, возникает, когда железо или металлические сплавы, содержащие железо, например сталь, подвергаются воздействию кислорода и воды в течение длительного периода времени.
Ржавчина образуется, когда железо подвергается процессу окисления, но не при любом окислении образуется ржавчина. Как указывалось ранее, только железо или сплавы, содержащие железо, могут ржаветь, но и другие металлы могут подвергаться коррозии аналогичным образом.
Что такое коррозия?
Коррозия возникает, когда элемент, который легко теряет свои электроны (например, некоторые металлы), соединяется с элементом, который поглощает дополнительные электроны (кислород), а затем вступает в контакт с раствором электролита (водой). Работа воды в процессе коррозии заключается в ускорении потока электронов от металла к кислороду.
Этот процесс называется окислительно-восстановительной реакцией и на самом деле представляет собой два химических процесса, протекающих одновременно: восстановление и окисление.
Что такое редукция?
Восстановление — это название химической реакции, которая происходит, когда молекула получает электрон. Это роль кислорода в коррозии металлов.
Что такое окисление?
Окисление противоположно восстановлению и является названием химической реакции, которая происходит, когда молекула теряет электрон. Это роль металла в коррозии металлов. Ржавчина и патина (странный зеленый цвет) меди — видимые результаты того, что металлы теряют свои электроны в воздухе.
Ржавеют ли медь, железо и алюминий?
Технически ржаветь может только железо и сплавы, содержащие железо. Другие металлы, в том числе драгоценные металлы, такие как золото и серебро, могут подвергаться коррозии аналогичным образом.
Что отличает некоторые металлы, так это продолжительность времени, необходимого для того, чтобы они начали ржаветь или подвергаться коррозии.
Вот несколько наиболее распространенных металлов и то, как они противостоят ржавчине и коррозии.
Медь ржавеет?
Медь не ржавеет, однако подвергается коррозии. Медь естественно коричневого цвета и приобретает ярко-зеленый оттенок по мере коррозии. Хотя некоторые считают реакцию меди скорее потускнением, чем окислением, металл все же подвергается аналогичному процессу «ржавчины».
В естественной среде медь крайне устойчива к коррозии. Тип коррозии, который в конечном итоге разрушает медные питьевые трубы, называется эрозионной коррозией, и он возникает только из-за воздействия проточной турбулентной воды в течение длительного периода времени.
Знаменитая красивая зеленая «патина», которую обычно можно увидеть на старых монетах, может полностью сформироваться в течение 20 лет.
Это один из немногих металлов, встречающихся в природе в качестве непосредственно используемого металла, а не добываемого из руды (хотя его можно получить и другими способами). Это, а также тот факт, что медь очень мягкая и с ней легко работать, привели к тому, что она стала одним из первых металлов, с которыми люди работали в истории человечества.
Это, а также тот факт, что медь очень мягкая и с ней легко работать, привели к тому, что она стала одним из первых металлов, с которыми люди работали в истории человечества.
На самом деле, медь была настолько важным делом, что у нас фактически есть период в истории, называемый Медным веком.
Медь хорошо проводит тепло и электричество, по этой причине она обычно используется в электропроводке.
Это также очень низкая в ряду реактивности, инструмент в химии, который представляет собой последовательность металлов, расположенных от самой высокой до самой низкой реакционной способности по отношению к кислотам, воде, извлечению металлов из их руд и другим реакциям. Из-за низкой реакционной способности особый сплав меди (90% меди и 10% никеля) используется для деталей лодок, которые будут подвергаться воздействию морской воды, или в качестве труб для транспортировки питьевой воды. Если вы посмотрите вокруг своего дома или здания, вы заметите, что многие из ваших приборов используют медные трубы для подачи и отвода воды.
По данным Министерства жилищного строительства и городского развития США, в среднем медная водопроводная труба должна прослужить 50-70 лет.
Ржавеет ли железо?
Да. Помните, что технически только железо и сплавы, содержащие железо, могут ржаветь.
По сравнению с коррозией других металлов железо ржавеет относительно быстро, особенно если подвергается воздействию воды и кислорода. Фактически, когда железо подвергается воздействию воды и кислорода, оно может начать ржаветь в течение нескольких часов.
Железо также быстро ржавеет, если подвергается воздействию высоких температур. Экстремальные температуры могут изменить химический состав металла, что делает его чрезвычайно склонным к рекомбинации с кислородом в окружающей среде.
Ржавеет ли алюминий?
Алюминий — один из наиболее часто используемых металлов на планете, и, возможно, он известен тем, что не ржавеет. Алюминий не ржавеет, только специфическое окисление железа называется ржавчиной, и при создании алюминия железо не используется. Однако, как и все металлы, алюминий подвержен коррозии.
Однако, как и все металлы, алюминий подвержен коррозии.
Алюминий производится в 3 этапа:
Этап 1. Добыча полезных ископаемых
Этап 2. Обработка
Этап 3. Электролитическое восстановление (которое создает настоящий алюминий)
Алюминий получают из минерала, называемого бокситом. Бокситы чаще всего встречаются в субтропических регионах, таких как Африка, Вест-Индия, Южная Америка и Австралия, хотя есть небольшие месторождения и в других местах, таких как Европа. Австралия является крупнейшим производителем бокситов, обеспечивая около 23% мирового производства.
Этот боксит затем перерабатывается в оксид алюминия, который просто состоит из атомов алюминия и кислорода, связанных вместе.
Через оксид алюминия проходит электрический ток, который отделяет различные компоненты друг от друга. На одном конце образуются пузырьки кислорода, а на другом конце собираются капли чистого расплавленного алюминия.
Около 4-5 тонн бокситов перерабатывается в 2 тонны оксида алюминия, что дает 1 тонну чистого алюминия.
Алюминий подвергается коррозии намного медленнее, чем другие металлы, такие как железо. Согласно Стэнфорду, причина, по которой алюминий не так легко подвергается коррозии, как другие металлы, заключается в особой реакции, которую он имеет с водой.
Обычно, когда вода вступает в контакт с металлом, она побуждает металл еще быстрее отдавать свои электроны кислороду вокруг него.
Однако алюминий имеет особую реакцию на воду. Когда вода соприкасается с алюминием, атомы алюминия и кислорода (содержащиеся в металле, а не кислород в окружающем его воздухе) отдаляются друг от друга.
Они окажутся почти на 50 % дальше друг от друга, чем в начале. Эта реакция удаления изменяет молекулярную структуру алюминия ровно столько, сколько , чтобы он стал химически инертным, что означает, что он не так легко подвергается коррозии.
Как защитить металлы от ржавчины
Ржавчина — это естественная химическая реакция. Несмотря на то, что некоторые металлы ржавеют быстрее, чем другие, это не должно удерживать вас от использования этих металлов для определенных целей. Есть много способов предотвратить ржавчину ваших металлов, например, краски и покрытия для металлов, жертвенные барьеры, барьерные пленки, а также многочисленные антикоррозионные решения и лужение. В каждом методе используются разные соединения и материалы для создания защитного барьера между металлом и элементами, вызывающими ржавчину и коррозию.
Несмотря на то, что некоторые металлы ржавеют быстрее, чем другие, это не должно удерживать вас от использования этих металлов для определенных целей. Есть много способов предотвратить ржавчину ваших металлов, например, краски и покрытия для металлов, жертвенные барьеры, барьерные пленки, а также многочисленные антикоррозионные решения и лужение. В каждом методе используются разные соединения и материалы для создания защитного барьера между металлом и элементами, вызывающими ржавчину и коррозию.
Узнайте, какие металлы здесь НЕ ржавеют.
Для получения дополнительной информации о том, как предотвратить ржавчину, посетите наши блоги: Как защитить сталь и железо от коррозии Steel and Supply for Quality Steel and Metal Если вы не уверены, какой металл подходит для вашего следующего проекта, обратитесь к профессионалам Tampa Steel & Supply. Наш обученный персонал поможет вам выбрать лучший металл для вашего следующего проекта. Кроме того, Tampa Steel & Supply может помочь вам предотвратить развитие ржавчины на ваших металлах на долгие годы! Свяжитесь с нами сегодня для всех ваших потребностей в стали.
